题目内容
【题目】学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。
(猜想)Ⅰ. 氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后________________________。
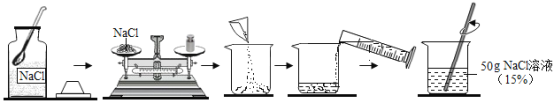
(实验)天平称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
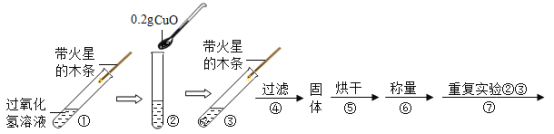
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
溶液中有气泡放出,带火星的木条复燃。 | 称量氧化铜质量为___________________。 | ________________。 | 猜想Ⅰ、Ⅱ不成立: 猜想Ⅲ成立。 |
(2)步骤⑦的目的是验证________________________。
【答案】质量和化学性质不变 0.2g 溶液中有气泡放出,带火星的木条复燃 氧化铜的化学性质在反应前后没有发生改变
【解析】
猜想:
Ⅲ、催化剂的特点是“一变,两不变”,即反应速率变,反应前后质量和化学性质不变。
实验:
(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故步骤③中的现象是有气泡产生,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以步骤⑥中称量的氧化铜的质量仍为0.2g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以⑦的现象是溶液中有气泡放出,带火星的木条复燃;故有:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
溶液中有气泡放出,带火星的木条复燃。 | 称量氧化铜质量为0.2g。 | 溶液中有气泡放出,带火星的木条复燃。 | 猜想Ⅰ、Ⅱ不成立: 猜想Ⅲ成立。 |
(2)步骤⑦的目的是验证氧化铜的化学性质在反应前后没有发生改变。