题目内容
【题目】2015年9月3日,我国举行了隆重的纪念抗战胜利70周年阅兵活动,其中包含许多化学知识,请用所学化学知识回答下列问题.
(1)阅兵礼炮为活动拉开了序幕,礼炮炮身(特殊钢材)涂刷了油漆,不仅使炮身变得美观,还可防锈,铁会生锈属于铁的__(填“化学”或“物理”)性质.鸣放时无外抛物,无环境污染.下列属于空气污染物的是__.
A 二氧化硫 B 一氧化碳 C 二氧化碳 D 氮气
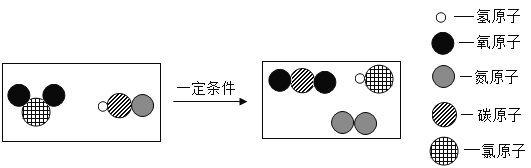
(2)空中梯队飞过天安门上空时,拉出一条条彩色烟带.产生烟带的药品除了燃料外还有锌、氯化铵、三硫化锑等.
①氯化铵受热分解的化学方程式为NH4Cl![]() X↑+HCl↑,则X的化学式是__.
X↑+HCl↑,则X的化学式是__.
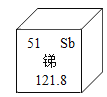
②如图是锑元素在周期表中的信息,下列说法正确的是__.
A 锑属于非金属元素
B 锑的相对原子质量为121.8
C 锑原子的中子数为51
D 三硫化锑的化学式为SbS3.
【答案】化学 AB NH3 B
【解析】
(1)铁生锈有主要成分是氧化铁的新物质生成,所以铁会生锈属于铁的化学性质,空气污染物主要二氧化硫、二氧化氮、一氧化碳、臭氧、可吸入用颗粒物,故填:化学;AB。
(2)①NH4Cl ![]() X↑+HCl↑,反应前含有1个N原子,4个H原子,1个Cl原子,反应后含有1个H原子,1个Cl原子,故X中含有1个N原子和3个H原子,所以其化学式为NH3,故填:NH3。
X↑+HCl↑,反应前含有1个N原子,4个H原子,1个Cl原子,反应后含有1个H原子,1个Cl原子,故X中含有1个N原子和3个H原子,所以其化学式为NH3,故填:NH3。
②A、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是锑,属于金属元素,故错误。
B、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为121.8,故正确。
C、根据元素周期表中的一格可知,左上角的数字为51,表示原子序数为51,根据原子序数=核电荷数=质子数=核外电子数,中子数+质子数≈相对原子质量,中子数≈121.8-51=70.8,故错误。
D、硫元素的化合价是﹣2价,所以三硫化锑的化学式为Sb2S3,故错误。
故选:B。

 阅读快车系列答案
阅读快车系列答案【题目】化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究。
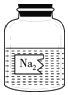
(提出问题)这是一瓶什么溶液?
(猜想与假设)海天同学的猜想是Na2SO3溶液;刘浩同学的猜想是Na2SO4溶液;你的猜想是_____(写一种)。
(查阅资料)
Ⅰ.白色沉淀BaSO3不溶于水,但要溶于稀盐酸。
Ⅱ.硝酸具有强氧化性,能将BaSO3氧化成BaSO4。
Ⅲ.Na2SO3与稀盐酸反应产生SO2,SO2能使石灰水变浑浊,也能使品红溶液褪色。
(进行实验)
Ⅰ.海天同学取适量的该溶液于试管中,滴加稀盐酸,产生无色气体,他认为自己的猜想成立,而刘浩同学认为他的结论不合理,原因是_____。
Ⅱ.刘浩同学为了验证自己的猜想,做了如下实验:
取适量的该溶液于试管中,先滴加足量的BaCl2溶液,再滴加过量稀硝酸,现象为_____,刘浩同学认为自己的猜想成立。
Ⅲ.卓玛同学对刘浩同学的猜想又提出了质疑,她认为加BaCl2和稀硝酸,Na2SO3也会产生沉淀,为了验证自己的观点,做了如下实验:
步骤 | 操作 | 实验现象 | 实验结论 |
步骤1 | 取少量该溶液于试管中,滴加足量的BaCl2溶液 | _______ | 无 |
步骤2 | 向步骤1的试管中滴加足量的稀盐酸 | _______ | 此溶液不是Na2SO4 |
步骤3 | 将步骤2中产生的气体通入品红溶液 | 品红溶液褪色 | _______ |
写出卓玛同学实验过程中的化学方程式:___________,__________。
【题目】某校化学兴趣小组在探究“酸碱盐的相关性质”时,做了如图一所示的两个实验,实验结束后,小组同学将两支试管中的废液同时倒入一个洁净的烧杯中(如图所示),观察到有气泡产生,为确认烧杯内溶液中溶质的成分,同学们进行了如下探究。
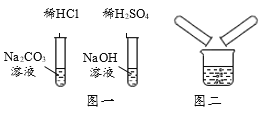
(查阅资料)Na2SO4溶液、NaCl溶液呈中性。
(提出猜想)猜想1:Na2SO4、NaCl;
猜想2:Na2SO4、NaCl和_____;
猜想3:Na2SO4、NaCl和H2SO4;
猜想4:Na2SO4、NaCl、H2SO4和Na2CO3。
(交流讨论)小强同学认为猜想4一定是错误的,他的理由是_____(用化学方程式表示)。
(进行实验)小明同学设计如下两个实验方案:
实验步骤 | 实验现象 | 实验结论 | |
方案一 | 取少量烧杯中的溶液于洁净的试管中,加入几滴紫色石蕊溶液 | _____ | 猜想3正确 |
方案二 | 取少量烧杯中的溶液于洁净的试管中,加入少量铁粉 | _____ |
请写出方案二中有关反应的化学方程式:_____。
(反思与总结)分析反应后溶液中溶质成分,除要考虑生成物外,还需考虑反应物是否过量。
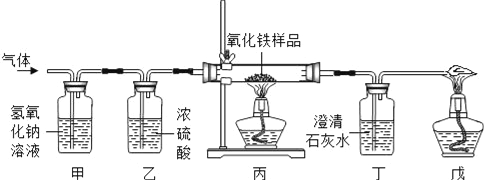
【题目】为了检测某石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得据如下表:
甲同学 | 乙同学 | 丙同学 | 丁同学 | |
所取石灰石样品质量(g) | 12.5 | 12.5 | 12.5 | 12.5 |
加入盐酸的质量(g) | 30.0 | 40.0 | 55.0 | 70.0 |
剩余固体的质量(g) | 6.5 | 4.5 | 2.5 | 2.5 |
试回答:
①样品中碳酸钙的质量分数为多少?.
②12.5g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程)
【题目】化学实验室常用二氧化锰催化过氧化氢分解的方法制取氧气。那么,影响过氧化氢分解快慢的因素到底有哪些呢?某化学兴趣小组对此进行如下研究。
(提出问题)影响过氧化氢分解快慢的因素有哪些?
(猜想与假设)假设1:过氧化氢溶液的浓度;
假设2:催化剂的质量;
假设3:温度;
假设4:_______。
(设计实验)小明同学设计如下实验方案进行验证。
序号 | H2O2溶液的浓度 | H2O2溶液的质量 | 温度 | MnO2的质量 | 收集O2的体积 | 时间 |
① | 5% | 12 g | 20 ℃ | 0.2 g | 125 mL | 20 s |
② | 30% | 12 g | 20 ℃ | 0.2 g | 125 mL | 2 s |
③ | 30% | 12 g | 40 ℃ | 无 | 125 mL | 148 s |
(1)通过对比实验①和②可知,过氧化氢分解的快慢与_______有关。
(2)在过氧化氢分解前后,二氧化锰的质量和_______不变。
(3)请你写出用二氧化锰催化过氧化氢分解的化学方程式:_______。
(讨论交流)(4)小红同学认为在这个实验中,必须用排水法收集氧气,理由是_______。
(5)小辉同学提出小明的方案无法验证温度对过氧化氢分解快慢的影响,请你帮他说出理由:____。
(拓展延伸)同学们查阅资料得知,FeCl3溶液对过氧化氢分解也有影响。在老师的指导下设计实验继续探究,向两支试管中分别加入等质量、不同浓度的H2O2溶液,再加入等质量、等浓度的FeCl3溶液,分别用气压传感器测定两试管中气体压力的变化曲线,如图1。
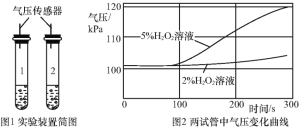
(6)为保证实验的准确性,请你设计向两试管中加入FeCl3溶液的具体方法:__。
(7)请你从图2曲线中找出FeCl3溶液对H2O2分解影响的两条规律性结论:__;____。