题目内容
【题目】化学实验室常用二氧化锰催化过氧化氢分解的方法制取氧气。那么,影响过氧化氢分解快慢的因素到底有哪些呢?某化学兴趣小组对此进行如下研究。
(提出问题)影响过氧化氢分解快慢的因素有哪些?
(猜想与假设)假设1:过氧化氢溶液的浓度;
假设2:催化剂的质量;
假设3:温度;
假设4:_______。
(设计实验)小明同学设计如下实验方案进行验证。
序号 | H2O2溶液的浓度 | H2O2溶液的质量 | 温度 | MnO2的质量 | 收集O2的体积 | 时间 |
① | 5% | 12 g | 20 ℃ | 0.2 g | 125 mL | 20 s |
② | 30% | 12 g | 20 ℃ | 0.2 g | 125 mL | 2 s |
③ | 30% | 12 g | 40 ℃ | 无 | 125 mL | 148 s |
(1)通过对比实验①和②可知,过氧化氢分解的快慢与_______有关。
(2)在过氧化氢分解前后,二氧化锰的质量和_______不变。
(3)请你写出用二氧化锰催化过氧化氢分解的化学方程式:_______。
(讨论交流)(4)小红同学认为在这个实验中,必须用排水法收集氧气,理由是_______。
(5)小辉同学提出小明的方案无法验证温度对过氧化氢分解快慢的影响,请你帮他说出理由:____。
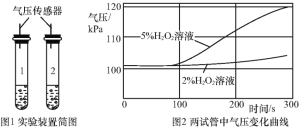
(拓展延伸)同学们查阅资料得知,FeCl3溶液对过氧化氢分解也有影响。在老师的指导下设计实验继续探究,向两支试管中分别加入等质量、不同浓度的H2O2溶液,再加入等质量、等浓度的FeCl3溶液,分别用气压传感器测定两试管中气体压力的变化曲线,如图1。
(6)为保证实验的准确性,请你设计向两试管中加入FeCl3溶液的具体方法:__。
(7)请你从图2曲线中找出FeCl3溶液对H2O2分解影响的两条规律性结论:__;____。
【答案】催化剂的种类(合理即可) 过氧化氢溶液的浓度 化学性质 2H2O2![]() 2H2O+O2↑ 排水法能准确测定收集氧气的体积 方案中没有温度不同,其他变量全部相同的对照实验 分别用注射器吸取等量、等浓度的氯化铁溶液,同时注入两支试管中 氯化铁溶液能加快过氧化氢的分解 氯化铁溶液对浓度大的过氧化氢溶液催化效果更好
2H2O+O2↑ 排水法能准确测定收集氧气的体积 方案中没有温度不同,其他变量全部相同的对照实验 分别用注射器吸取等量、等浓度的氯化铁溶液,同时注入两支试管中 氯化铁溶液能加快过氧化氢的分解 氯化铁溶液对浓度大的过氧化氢溶液催化效果更好
【解析】
[作出假设]影响过氧化氢溶液分解快慢的因素可能有过氧化氢溶液的浓度、催化剂的质量、催化剂的种类以及温度;
[设计实验](1)实验①和②中除了过氧化氢溶液的浓度不同以外,其他条件均相同,通过实验数据分析可知,过氧化氢溶液分解的快慢与过氧化氢溶液的浓度
有关系;
(2)二氧化锰在过氧化氢溶液分解中充当催化剂,在反应前后质量和化学性质不变;
(3)过氧化氢在二氧化锰的催化作用下分解为水和氧气;反应的化学方程式:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
[讨论交流](4)用排水法收集氧气便于观察到氧气是否收集满;
(5)所设计的三组实验中,没有除了温度不同以外,其他条件均相同的对比实验,所以无法验证温度对过氧化氢溶液分解快慢的影响;
[拓展延伸](6)向试管中加入FeCl3溶液,可以分别用注射器吸取等量、等浓度的FeCl3溶液同时注入两支试管中;
(7)根据曲线可以看出,FeCl3溶液能加快H2O2溶液的分解;FeCl3溶液对浓度大H2O2溶液分解促进效果更好。

【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法不正确的是( )
物质 | X | Y | Z | W |
反应前质量/g | 10 | 3 | 90 | 0 |
反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
A. W可能是单质 B. Y可能是催化剂
C. 该反应是分解反应 D. 反应后Z物质的质量为![]()
【题目】过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
I.不稳定性
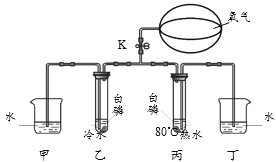
(1)如下图所示进行实验,过氧化氢分解的化学方程式为_______________,产生3.2g O2时分解的过氧化氢的质量为______ g。

(2)能用排水法收集O2的原因是______。
(3)探究温度对过氧化氢分解速率的影响
同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度% | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40min | 40min | 40 min |
由此得出的结论是_____________________________。
Ⅱ.腐蚀性
【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
将铜片分别浸泡在3种溶液中进行实验,如下表。
编号 | ① | ② | ③ |
实验 |
|
|
|
一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
【解释与结论】
(4)实验①的作用是_____________________。
(5)铜片被腐蚀的反应如下,补全该反应的化学方程式。
Cu + H2O2+ H2SO4=== CuSO4 +_______。
【反思交流】
(6)某同学提出,实验②中,除发生(5)的反应外,还发生了一个反应导致有细小气泡产生,该反应的反应物为_______。