题目内容
【题目】二氧化氯(ClO2)在生产、生活中具有广泛应用.
(1)ClO2可用于工业制备高效氧化剂、漂白剂亚氯酸钠(NaClO2).
①ClO2中氯元素的化合价为_______.
②工业生产NaClO2的主要反应的化学方程式为2ClO2+2X![]() Cl2+2NaClO2 , 其中X的化学式为________.
Cl2+2NaClO2 , 其中X的化学式为________.
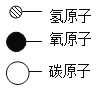
(2)ClO2是国际上公认的安全、无毒的消毒剂,可以快速将剧毒的氰化物氧化.ClO2与氰化氢(HCN)在气态下反应的微观示意图如下:
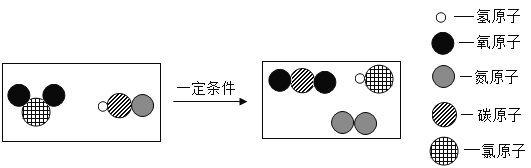
该反应生成的N2与CO2的质量比为________.
【答案】+4 NaCl 7:22
【解析】
(1)①氧显﹣2价,设二氧化氯中氯元素的化合价为x,根据在化合物中正负化合价代数和为零,则:x+(﹣2)×2=0,得x=+4,故填:+4;
②根据化学变化前后原子的种类、数目不变,X的2个分子中含有2个Na原子和2个Cl原子,则每个X分子由1个Na原子和1个Cl原子构成,则X的化学式为NaCl;
(2)HClO2与氰化氢(HCN)在气态下反应的方程式是2ClO2+2HCN N2+2CO2+2HCl,该反应生成的N2与CO2的质量比为28:(44×2)=7:22。
N2+2CO2+2HCl,该反应生成的N2与CO2的质量比为28:(44×2)=7:22。

【题目】化学是从微观角度研究物质的组成、结构及其变化的科学。
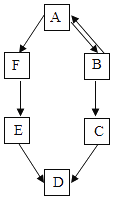
(1)构成物质的粒子之间的关系如图1所示,请回答下列问题:
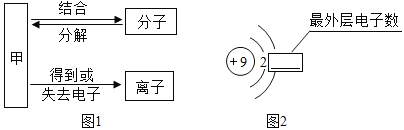
①A是________________。
②图2是氟元素的原子结构示意图,方框横线上的数字是________________,在化学反应中易__________电子(填“得到”或“失去”)。
③保持氯化氢气体化学性质的最小粒子是_______________(填符号)。
(2)己知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则核外电子数为___________。
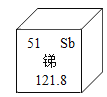
(3)如图是钠元素和氟元素在元素周期表中的信息。

由此信息得出:
① 钠元素的原子序数是________________。
②由钠元素与氟元素组成氟化钠的化学式为________________。
(4)甲、乙、丙、丁表示四种物质,部分物质的微观示意图见下表。甲和乙在一定条件下反应生成丙和丁。
物质 | 甲 | 乙 | 丙 | 丁 |
|
微观示意图 | 化合物 |
|
|
|
请回答:若一定质量的化合物甲和48g的乙恰好完全反应,可生成44g丙和27g丁,则甲的化学式是________________。
【题目】阅读下面的科普短文。
中国有很长的饮茶历史,茶叶中含有茶多酚等物质。
茶多酚是从天然茶叶中提取的混合物,由儿茶素、黄酮苷类、酚酸等组成,是一种白色粉末,略有吸水性。易溶于温水、乙醇等,在碱性环境中不稳定。茶多酚容易被氧化变色,下图是多酚氧化酶催化茶多酚氧化的示意图(图中a、b、c、d分别代表4种物质)。

研究发现,茶多酚是茶叶发挥健康保健功效最主要的物质,最典型的代表是儿茶素,具有抗氧化(消除氧自由基)、抗炎、降低心血管病发病几率、预防癌症、降血脂、减少体脂形成、抗菌、改变肠道菌群生态等多项功效。研究表明,喝下一杯茶半小时后,血中的抗氧化容量(对抗氧自由基的能力)增加41%﹣48%,并能在高水平状态持续一个半小时。
茶多酚还可用于食品保鲜防腐,根据我国《食品添加剂使用卫生标准》规定茶多酚的使用范围和使用量如下:
食物 | 不含水的脂肪和油 | 熟坚果 | 油炸面制品 | 燕麦片 | 方便面 |
含量(g/kg) | 0.4 | 0.2 | 0.2 | 0.2 | 0.2 |
溶剂法是从茶叶中提取茶多酚的传统方法之一,利用茶多酚和茶叶中其他成分在乙醇中的溶解度不同进行分离。具体的方法是将茶叶用乙醇浸渍,然后把浸取液进行液﹣液分离,最后浓缩得到产品。
依据文章内容回答下列问题。
(1)根据以上描述请你归纳茶多酚的物理性质有_________________。
(2)多酚氧化酶催化茶多酚氧化的过程中,其中代表酶的是_________________
A a B b C c D d
(3)若一包方便面的质量是100g,则最多加入茶多酚保鲜剂_________________mg。
(4)下列关于茶多酚的说法中,正确的是_________________
A 茶多酚在碱性环境中不稳定
B 适量喝茶有益身体健康
C 利用溶剂法提取茶多酚属于化学变化
D 某同学在中午12点喝了一杯茶,他血中的抗氧化容量的较高水平可持续到14点
(5)保存茶多酚晶体时应注意_________________。
【题目】对下列概念的理解或相关说法中正确的是
选项 | 概念 | 解释或说法 |
A | 置换反应 | 一定有元素化合价发生变化的反应 |
B | 化合物 | 含有 |
C | 中和反应 | 只要是生成盐和水的反应都是中和反应 |
D | 离子 | 带电的微粒 |
A.AB.BC.CD.D