题目内容
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
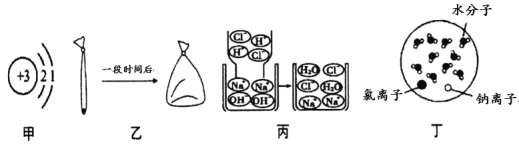
(1)甲图为锂原子(Li)结构示意图,锂原子在化学反应中容易____(填“得”或“失”)电子。锂的氧化物的化学式为_____________。
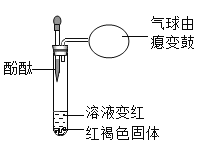
(2)如乙图所示,将一小块干冰放进一个塑料袋,将袋口扎紧,一段时间后,塑料袋鼓起。从微观角度分析,塑料袋鼓起的主要原因是______________________________________________。干冰可做食品制冷剂,利用了干冰的性质是____________________________________________。
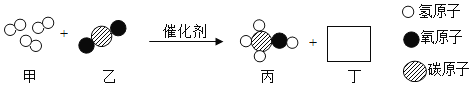
(3)从微粒的角度说明图丙化学反应的实质是_________________________________________。
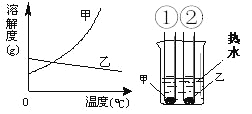
(4)丁图表示t℃时,某溶液的微观模型,该溶液中溶质是_________,该溶液中溶质和溶剂的质量比为_____________________(最简整数比)。
【答案】失 Li2O 分子间的间隙变大了 干冰升华时能够吸收热量 H+和OH-结合成H2O或氢离子和氢氧根离子结合成水分子 NaCl 13:40
【解析】
(1)锂原子最外层有1个电子,电子个数小于4在化学变化中易失去电子,而形成带1个单位正电荷的锂离子,Li的化合价为+1价,O的为-2价,故锂的氧化物的化学式为Li2O;
(2)从分子的角度分析,塑料袋鼓起的原因是,分子间存在间隙,二氧化碳由固态变为气态时,分子间的间隙变大了;干冰做制冷剂,主要是利用干冰升华时能够吸收热量的物理性质;
(3)从图丙可知,该反应的微粒在反应前后的变化是:反应前存在钠离子、氢氧根离子、氯离子、氢离子四种离子,反应后存在钠离子、氯离子和水分子。从微粒的角度说明图丙反应的实质是H+和OH-结合成H2O或氢离子和氢氧根离子结合成水分子;
(4)从丁图可知为氯化钠溶液,在氯化钠溶液中,溶质是NaCl,溶剂是水;由图丁可知含有1个钠离子和1个氯离子以及10个水分子,则溶质氯化钠的质量:溶剂水的质量=(23+35.5):10×18=13:40。

 走进文言文系列答案
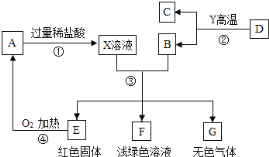
走进文言文系列答案【题目】X、Y、Z、W 四种物质的转化关系如图所示(“ →”表示反应一步实现,部分物质和反应条件已略去),则符合要求的X、Y、Z、W 依次是
![]()
选项 | X | Y | Z | W |
A | Al | Cu | CuO | CuSO4 |
B | HCl | NaCl | Na2CO3 | NaOH |
C | H2O2 | O2 | H2O | H2CO3 |
D | Fe2O3 | FeCl3 | Fe(OH)3 | Fe |
A. AB. BC. CD. D
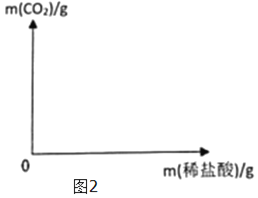
【题目】某未知气体X可能含有CO、CH4中的一种或两种,某同学设计实验进行探究。
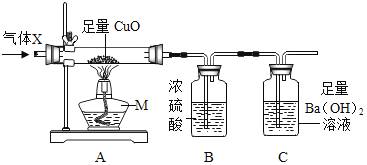
查阅资料:
(ⅰ)加热时,CH4能与CuO反应生成Cu、CO2和H2O;
(ⅱ)20℃时,100g水中分别能溶解Ca(OH)2和Ba(OH)2分别为:0.165g,2.1g;
(iii)结构决定性质,Ba(OH)2结构与Ca(OH)2相似,也能与CO2反应。
(iv)浓硫酸具有吸水性。
(1)CH4与CuO反应的化学方程式为______。
(2)气体X成分的猜想与探究
猜想1:只有CO猜想2:只有CH4猜想3:______。
小明依据猜想进行如下实验:
实验操作 | 实验现象 | 实验结论 |
①实验时,先往装置中通一段时间的N2 ②再通入气体X后加热 | ①A中玻璃管内黑色粉末逐渐变红 ②B瓶增重,C中出现浑浊 | 可知猜想 ______ 不成立 |
(3)讨论与反思:①先通N2的目的是______。
②根据上述变化仍无法确定气体X的成分,还需要测定______(填序号),并进行定量分析才能得出结论
a.实验前A中CuO的质量 b.B瓶增重的质量 c.C瓶增重的质量
③C中用Ba(OH)2溶液而不用Ca(OH)2溶液的原因是______。
④从环保的角度,该装置还应进行的改进是______。