题目内容
【题目】铜陵地区的石灰石储量丰富。某化学兴趣小组取12.5g石灰石样品(样品中杂质不溶于水,也不与酸反应)粉碎后放入烧杯,然后向其中加入100g稀盐酸恰好完全反应,得到108.1g剩余物,请计算:
(1)产生CO2的质量为_____ g;
(2)该石灰石样品中碳酸钙的质量分数_____。
【答案】4.4g 80%
【解析】
(1)反应前烧杯中物质的总质量为12.5g+100g=112.5g,反应后烧杯内物质的质量变为108.1g,
由质量守恒可知,二氧化碳的质量为112.5g﹣108.1g=4.4g,
(2)设碳酸钙的质量为x,
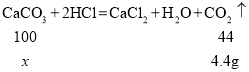
![]()
解得x=10g,
该样品中碳酸钙的质量分数为![]() ×100%=80%,
×100%=80%,
故答案为:(1)4.4 (2)石灰石样品中碳酸钙的质量分数是80%;

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
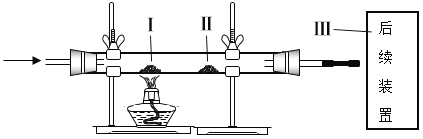
【题目】为探究影响氯酸钾分解速率的因素,小红同学把实验温度恒定在330℃或380℃,(其他实验条件见下表),并设计了以下实验。
实验编号 | 氯酸钾的质量 | 其他物质的质量∕g | 温度∕℃ | 收集氧气的体积/mL | 反应所需时间∕s |
① | 2.0 | 330 | 100 | t1 | |
② | 2.0 | CuO 0.5 | 330 | 100 | t2 |
③ | 2.0 | MnO2 0.5 | 330 | 100 | t3 |
④ | 2.0 | MnO2 ____ | _______ | 100 | t4 |
请回答
(1)进行实验②和③,并对对比,其实验目的是____________________。
(2)要说明氧化铜对氯酸钾分解速率的影响,则要选用实验______和实验_______进行对比。
(3)用实验③和④探究温度对氯酸钾分解速率的影响,则MnO2的质量是__________g,反应的温度是_________℃,实验④发生反应的化学方程式为___________________;若t3>t4,氯酸钾分解速率与温度的关系是__________________。