题目内容
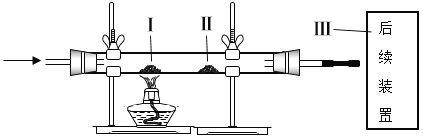
【题目】某未知气体X可能含有CO、CH4中的一种或两种,某同学设计实验进行探究。
查阅资料:
(ⅰ)加热时,CH4能与CuO反应生成Cu、CO2和H2O;
(ⅱ)20℃时,100g水中分别能溶解Ca(OH)2和Ba(OH)2分别为:0.165g,2.1g;
(iii)结构决定性质,Ba(OH)2结构与Ca(OH)2相似,也能与CO2反应。
(iv)浓硫酸具有吸水性。
(1)CH4与CuO反应的化学方程式为______。
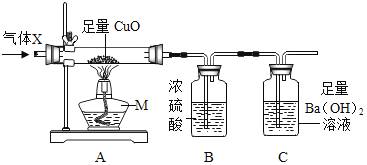
(2)气体X成分的猜想与探究
猜想1:只有CO猜想2:只有CH4猜想3:______。
小明依据猜想进行如下实验:
实验操作 | 实验现象 | 实验结论 |
①实验时,先往装置中通一段时间的N2 ②再通入气体X后加热 | ①A中玻璃管内黑色粉末逐渐变红 ②B瓶增重,C中出现浑浊 | 可知猜想 ______ 不成立 |
(3)讨论与反思:①先通N2的目的是______。
②根据上述变化仍无法确定气体X的成分,还需要测定______(填序号),并进行定量分析才能得出结论
a.实验前A中CuO的质量 b.B瓶增重的质量 c.C瓶增重的质量
③C中用Ba(OH)2溶液而不用Ca(OH)2溶液的原因是______。
④从环保的角度,该装置还应进行的改进是______。
【答案】CH4+4CuO![]() 4Cu+CO2+2H2O 既有CO又有CH4 1 排尽装置内的空气,防止空气和氧气的混合气加热发生爆炸 bc 氢氧化钡溶解度比氢氧化钙溶解度大,有利于全部吸收二氧化碳 点燃或收集尾气
4Cu+CO2+2H2O 既有CO又有CH4 1 排尽装置内的空气,防止空气和氧气的混合气加热发生爆炸 bc 氢氧化钡溶解度比氢氧化钙溶解度大,有利于全部吸收二氧化碳 点燃或收集尾气
【解析】
(1)甲烷和氧化铜在加热的条件下生成铜、二氧化碳和水,化学方程式为:CH4+4CuO![]() 4Cu+CO2+2H2O;
4Cu+CO2+2H2O;
(2)依据气体X成分的猜想可知,猜想3:既有CO又有CH4;
根据变化2可知,B瓶增重,说明反应生成了水,而一氧化碳和氧化铜反应不能生成水,所以猜想1不成立;
(3)①可燃性气体和助燃性气体,在点燃时,可能发生爆炸,所以先通N2的目的是:排尽装置内的空气,防止空气和氧气的混合气加热发生爆炸;
②上述变化仍无法确定气体X的成分,还需要测定b、c,并进行定量分析才能得出结论,这是因为B瓶增重的质量是反应生成水的质量(说明气体中一定含有甲烷),C瓶增重的质量是反应生成二氧化碳的质量,根据二氧化碳和水的质量比及其CH4+4CuO![]() 4Cu+CO2+2H2O中二氧化碳和水的质量比可以判断气体中是否含有一氧化碳;
4Cu+CO2+2H2O中二氧化碳和水的质量比可以判断气体中是否含有一氧化碳;
③C中用Ba(OH)2溶液而不用Ca(OH)2溶液的原因是氢氧化钡溶解度比氢氧化钙溶解度大,有利于全部吸收二氧化碳;
④一氧化碳有毒,需要尾气处理,所以该装置还应进行的改进是:点燃或收集尾气。
故答案为:(1)CH4+4CuO![]() 4Cu+CO2+2H2O;(2)既有CO又有CH4;1;(3)①排尽装置内的空气,防止空气和氧气的混合气加热发生爆炸;②bc;③氢氧化钡溶解度比氢氧化钙溶解度大,有利于全部吸收二氧化碳;④点燃或收集尾气。
4Cu+CO2+2H2O;(2)既有CO又有CH4;1;(3)①排尽装置内的空气,防止空气和氧气的混合气加热发生爆炸;②bc;③氢氧化钡溶解度比氢氧化钙溶解度大,有利于全部吸收二氧化碳;④点燃或收集尾气。