题目内容
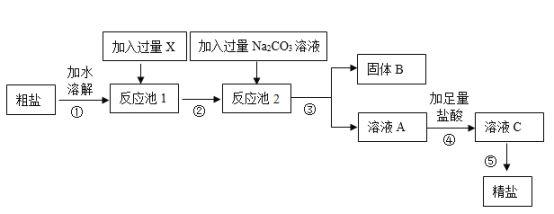
【题目】乙烯是重要的化工原料,实验室利用浓硫酸的脱水性。以乙醇为原料制取乙烯(![]() ),其反应的微观过程如图,对此下列有关说法中错误的是
),其反应的微观过程如图,对此下列有关说法中错误的是
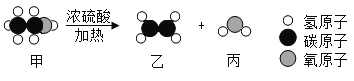
A.物质甲、乙都属于有机物
B.反应中原子的种类和个数不变
C.该反应属于分解反应
D.生成物乙和丙的质量比为![]()
【答案】D
【解析】
根据反应的微观模拟示意图,分析反应物、生成物,写出反应的方程式,根据方程式分析判断有关的问题。
由反应的微观模拟示意图可知,反应物甲是乙醇,生成物是乙是乙烯、丙是水,反应的方程式是:C2H5OH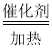 C2H4+H2O由此可知:
C2H4+H2O由此可知:
A、物质甲、乙都是含碳元素的化合物,都属于有机物,故正确;
B、对比反应前后原子的变化可知,化学反应前后原子的种类及数目都没有改变,故B正确;
C、该反应由一种物质生成了两种物质,属于分解反应,故正确;
D、生成物乙和丙的质量比为:(12×2+1×4):(1×2+16)=14:9,故错误。
故选:D。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
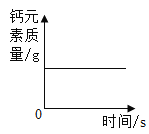
仁爱英语同步练习册系列答案【题目】取10g锌粉和铜粉的混合物于烧杯中,向烧杯中分四次加入等质量的同种稀硫酸,实验过程中得到如下数据。
第1次 | 第2次 | 第3次 | 第4次 | |
加入稀硫酸的质量 | 20g | 20g | 20g | 20g |
剩余固体的质量 | 8.7g | 7.4g | 6.1g | 5.5g |
(1)混合物中铜粉的质量是________。
(2)所用稀硫酸中溶质的质量分数是_____。(保留计算过程)
【题目】某校化学活动小组准备探究气体的测定和数据处理方法。
(提出问题)如何利用石灰石与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
(实验设计)通过下列两个实验分别测定CO2的质量和体积:
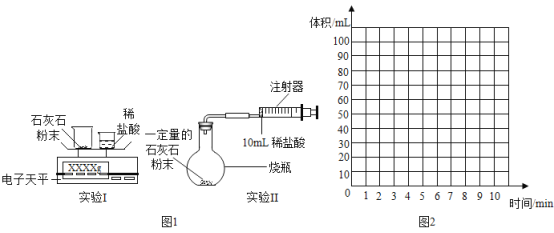
(分析与表达)
(1)上述两个实验中,反应的化学方程式为________。
(2)实验Ⅰ中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是________。
(3)实验Ⅱ中,先连接好装置,在检查装置的气密性(请简述方法________),然后装好药品,最后将10mL稀盐酸快速推入烧杯中,若稀盐酸是缓慢推入的,则可能造成的后果是________.
(4)(记录与处理)
已知实验Ⅰ反应前的总质量(m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)),要计算生成CO2的质量,至少还需要的数据是___________。
A m(小烧杯) B m(大烧杯) C m(大烧杯+反应后剩余物)
(5)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定)
时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
据以上实验过程和实验数据综合分析,最终生成CO2的体积是________ mL
注意:若答对下面题奖励4分,但化学总分不超过60分。
(6)根据你的认识,在图2中坐标图中绘制出0~10min生成CO2体积随时间变化的曲线。________
(7)(反思与评价)
经过分析,你认为实验Ⅰ的优点是________,实验Ⅱ的优点是________。
【题目】过氧化钠(![]() )是化学中常见的物质,为白至淡黄色的粉末状固体,易吸潮。与水发生反应生成氢氧化钠和具有氧化性的过氧化氢。
)是化学中常见的物质,为白至淡黄色的粉末状固体,易吸潮。与水发生反应生成氢氧化钠和具有氧化性的过氧化氢。
(1)写出过氧化钠与水的反应化学方程式 _____.
(2)为了验证过氧化钠与水反应生成了氢氧化钠,实验小组的同学将无色酚酞溶液滴到反应后的溶液中,观察到溶液变红又褪为无色。
(提出问题)什么原因使无色酚酞变红又褪色?
(猜想假设)小军:可能是无色酚酞溶液变质导致溶液褪色;
小敏:可能是氧气导致溶液褪色;
小花:_____.
(实验探究)A.小组同学都觉得小军的猜想不合理,原因_____.
B.小组同学用以下实验验证小敏和小花的猜想:
实验步骤 | 实验现象 | 实验结论 |
_____ | 无色酚酞溶液依然为红色 | 小敏猜想不正确 |
取少量稀氢氧化钠溶液于试管中,滴加 | _____ | 小花猜想正确 |