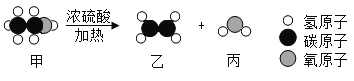题目内容
【题目】下列实验过程与图像描述不一致的是
A.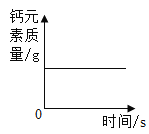 高温煅烧石灰石
高温煅烧石灰石
B.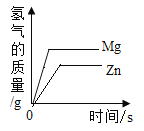 向等质量的镁、锌中分别加入足量稀硫酸
向等质量的镁、锌中分别加入足量稀硫酸
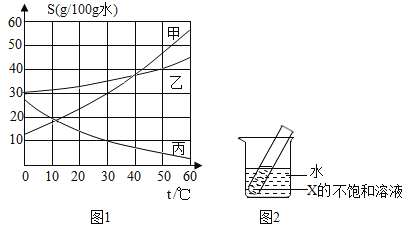
C. 室温下,向一定质量的饱和石灰水中加入生石灰
室温下,向一定质量的饱和石灰水中加入生石灰
D. 两份等质量、等质量分数的过氧化氢溶液在有无二氧化锰的情况下反应
两份等质量、等质量分数的过氧化氢溶液在有无二氧化锰的情况下反应
【答案】C
【解析】
A、高温煅烧石灰石,碳酸钙在高温的条件下分解为氧化钙和二氧化碳,根据质量守恒定律,化学反应前后,元素的质量不变,故钙元素的质量不变,不符合题意;
B、向等质量的镁、锌中分别加入足量稀硫酸,![]() ,
, ![]() ,镁的相对原子质量小于锌,故最后镁生成氢气的质量大于锌,不符合题意;
,镁的相对原子质量小于锌,故最后镁生成氢气的质量大于锌,不符合题意;
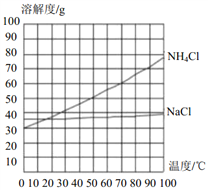
C、室温下,向一定质量的饱和石灰水中加入生石灰,氧化钙与水反应生成氢氧化钙,消耗了水分,且该反应放热,氢氧化钙的溶解度随温度的升高而减小,溶质的质量逐渐减小,冷却至室温的过程中,溶质质量又逐渐增大,待冷却至原温度时,由于消耗了水分,溶质质量小于原来质量,符合题意;
D、两份等质量、等质量分数的过氧化氢溶液在有无二氧化锰的情况下,有二氧化锰的生成氧气的速率较快,但是最后生成氧气的质量一样,不符合题意。
故选C。

【题目】某兴趣小组同学利用图1装置制取气体并探究气体的某些性质.
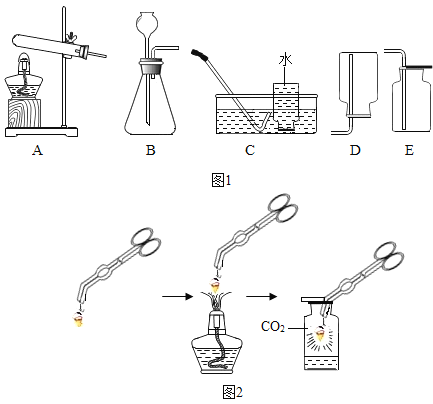
(1)制取气体
①若选择A与C组合制取氧气,反应的化学方程式为__.
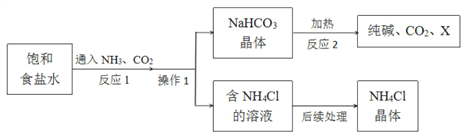
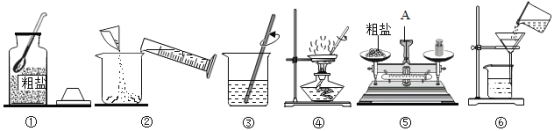
②用石灰石和稀盐酸制取CO2的化学方程式为__,选用的发生与收集装置是__(填标号).连接好装置,将药品加入装置前应进行的操作是__.
(2)探究气体的性质
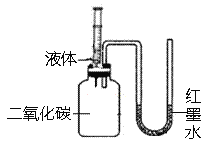
某同学在空气中点燃镁条,想利用CO2来熄灭燃烧的镁条,结果发现镁条在充满CO2的集气瓶中没有熄灭反而剧烈燃烧,集气瓶内壁出现黑色固体,瓶底出现白色固体,实验过程如图2所示.请回答:
①夹持镁条的仪器名称是__;
②生成的黑色固体是__(写化学式);
③查阅资料:MgO、Mg(OH)2、MgCO3均为难溶于水的白色固体.同学讨论后认为白色固体不可能是Mg(OH)2,理由是__.
④为进一步确定白色固体的成分,进行如下实验:
实验操作 | 实验现象 | 实验结论 |
取白色固体于试管中,加入足量稀盐酸 | __ | 白色固体不是MgCO3,而是MgO |
⑤镁在CO2中燃烧的化学方程式为__;通过上述探究,你对燃烧或灭火的新认识是__.