题目内容
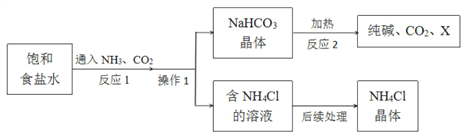
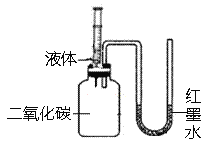
【题目】某校化学兴趣小组在实验室使用稀盐酸及某石灰石制取二氧化碳,反应后废物利用,用废水(含少量Fe3+等杂质)生产二水合氯化钙(CaC122H2O)。具体的实验流程如图所示,根据题意回答下列问题。
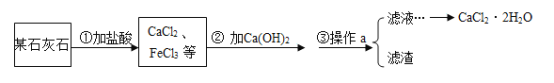
(1)写出第①步的化学方程式______。
(2)第②步发生的反应属于______反应(填基本反应类型)。
(3)操作a的名称是______。进行该操作时用到的玻璃仪器有烧杯、玻璃棒和______。
(4)滤渣的主要成分为______,它属于______(填物质分类)
【答案】CaCO3+2HCl=CaCl2+H2O+CO2↑ 复分解 过滤 漏斗 氢氧化铁 碱
【解析】
(1)第①步是石灰石的主要成分碳酸钙和盐酸反应生成氯化钙、水以及二氧化碳,对应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑。
(2)第②步是氯化铁和氢氧化钙反应,对应的化学方程式为2FeCl3+3Ca(OH)2=2Fe(OH)3↓+3CaCl2,属于复分解反应。
(3)操作a的结果是得到滤液和滤渣,由此可推得该操作为过滤。进行过滤操作时用到的玻璃仪器有烧杯、玻璃棒和漏斗。
(4)滤渣的主要成分为氢氧化铁,是金属离子和氢氧根离子形成的化合物,属于碱。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目