题目内容
【题目】(1)某研究性学习小组为验证“氨气还原氧化铜”的实验,认真阅资料并做出以下准备。
资料准备:I.氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,溶液呈碱性。
Ⅱ.氨气还原氧化铜的化学反应原理:2NH3+3CuO![]() 3Cu+N2+3H2O。
3Cu+N2+3H2O。
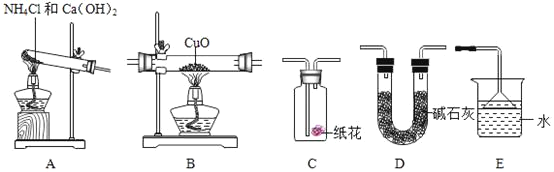
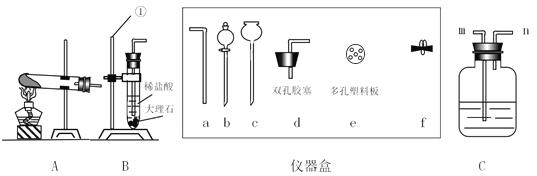
实验准备:
请回答:
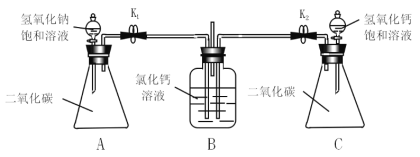
①为达成“氨气还原氧化铜”的实验目的,装置A、B、D、E的正确连接顺序_____;(填序号)
②装置A中发生反应的化学方程式_____;
③装置B观察到的现象_____,装置E的作用_____;
④将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变蓝色,原因是_____。
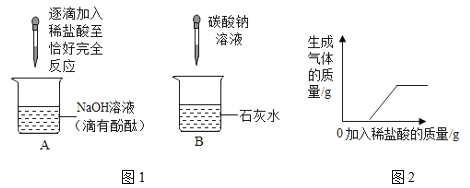
(2)金属镁可与热水反应生成氢氧化镁和氢气,所得溶液呈碱性,可使酚酞溶液显紅色。某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,变为红色,放置在空气中一段时间后,发现溶液的红色褪去了。
①镁与热水反应的化学方程式是_____。
②查阅资料:溶液红色褪去的原因是溶液碱性减弱。
(提出问题)导致溶液碱性减弱的原因是什么?
(假设与分析)
假设1:可能是氢氧化镁与N2或O2发生了反应。
假设2:可能是溶液吸收了空气中的_____。
假设3:可能是氢氧化镁的溶解度随温度的降低而_____。
由碱的性质可知,假设1不成立。
(实验探究)
实验操作 | 实验现象 | 结论 |
(1)取上述红色溶液,保持温度不变,在空气中放置一段时间,观察现象。 | _____ | 假设2成立 |
(2)取上述红色溶液,_____,_____,观察现象。 | 红色褪去 | 假设3成立 |
(拓展延伸)
③将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀。
请解释其原因:_____。
④除上述金属外,根据金属活动性顺序,预测_____也能跟硫酸铜溶液反应产生上述现象(举一例即可)。
【答案】A、D、B、E Ca(OH)2+2NH4Cl![]() CaCl2+2H2O+2NH3↑ 黑色氧化铜逐渐变成红色 吸收氨气,防止污染环境 氨气溶于水,形成氨水,氨水能使紫色石蕊显蓝色 Mg+H2O
CaCl2+2H2O+2NH3↑ 黑色氧化铜逐渐变成红色 吸收氨气,防止污染环境 氨气溶于水,形成氨水,氨水能使紫色石蕊显蓝色 Mg+H2O![]() Mg(OH)2+H2↑ CO2 减小 红色褪去 隔绝空气 冷却至室温(或放置一段时间至室温) 钠和水反应生成氢氧化钠和氢气,氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠 钾
Mg(OH)2+H2↑ CO2 减小 红色褪去 隔绝空气 冷却至室温(或放置一段时间至室温) 钠和水反应生成氢氧化钠和氢气,氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠 钾
【解析】
(1)①氢氧化钙和氯化铵在加热的条件下生成氯化钙、水和氨气,氨气溶于水形成氨水,碱石灰具有吸水性,氨气和氧化铜在加热的条件下生成铜、水和氮气,需要尾气处理。为达成“氨气还原氧化铜”的实验目的装置A、B、D、E的正确连接顺序:ADBE;
②装置A中发生的反应是氢氧化钙和氯化铵反应生成氯化钙、水和氨气,化学方程式为:Ca(OH)2+2NH4Cl![]() CaCl2+2H2O+2NH3↑;
CaCl2+2H2O+2NH3↑;
③根据氨气还原氧化铜的化学反应原理可知,氨气与黑色的氧化铜加热时生成红色的铜、氮气和水。装置B观察到的现象为:黑色氧化铜逐渐变成红色,装置E的作用是:吸收氨气,防止污染环境;
④将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变蓝色,原因是:氨气溶于水,形成氨水,氨水能使紫色石蕊显蓝色;
(2)①镁与热水反应生成氢氧化镁白色沉淀和氢气,反应的化学方程式为:Mg+H2O![]() Mg(OH)2+H2↑;
Mg(OH)2+H2↑;
②假设与
假设1:可能是氢氧化镁与N2或O2发生了反应;
空气中的二氧化碳与水反应生成碳酸,碳酸与氢氧化镁反应,溶液碱性减弱。假设2:可能是溶液吸收了空气中的二氧化碳;
溶液放置在空气中一段时间后,温度下降,氢氧化镁的溶解度降低,溶液碱性减弱。假设3:可能是氢氧化镁的溶解度随温度的降低而降低;
实验探究:
(1)取上述红色溶液,保持温度不变,在空气中放置一段时间,观察现象,溶液红色褪去,假设2成立;
(2)取上述红色溶液,隔绝空气,冷却至室温(或放置一段时间至室温),观察现象,红色褪去,假设③成立。故填:
实验操作 | 实验现象 | 结论 |
(1)取上述红色溶液,保持温度不变,在空气中放置一段时间,观察现象。 | 红色褪去 | 假设2成立 |
(2)取上述红色溶液,隔绝空气,冷却至室温(或放置一段时间至室温),观察现象。 | 红色褪去 | 假设3成立 |
拓展延伸:
③将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀,因为钠和水反应生成氢氧化钠和氢气,氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠。
②除上述金属外,根据金属活动性顺序,预测钾也能跟硫酸铜溶液反应产生上述现象,因为钾比钠活泼。