题目内容
【题目】根据下图回答问题。
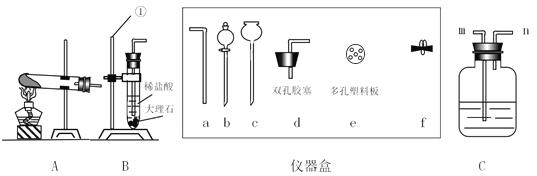
(1)仪器①的名称为_____。
(2)实验室可用于氯酸钾和二氧化锰制取氧气,反应前后,二氧化锰的质量 _____(填“不变”、“变大”或“变小”),其制备装置可以选择A,检查该装置气密性的方法是_____,若导管口有气泡冒出,则装置不漏气。
(3)实验室用大理石和稀盐酸制取二氧化碳,反应的化学方程式是_____,装置B是二氧化碳的制备装置,其中有_____处错误。如果要把装置B改装成可控制反应发生和停止的装置,要先取掉带导管的单孔胶塞,再从仪器盒中选择的仪器是_____(填字母)。
(4)图C可用于检验二氧化碳,反应方程式是_____,气体从_____口进(选“m”或“n”)。
(5)下图可验证氢氧化钠和氢氧化钙的性质:分別打开分液漏斗活塞,将等体积的氢氧化钠饱和溶液和氢氧化钙饱和溶液全部加入锥形瓶中,关闭活塞,打开弹簧夹K1、K2,观察实验现象。
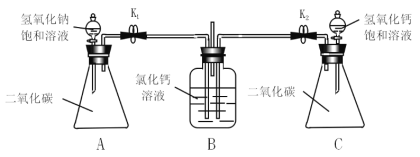
①在A装置中观察到_____的现象,证明氢氧化钠与二氧化碳确实发生了反应。
②实验后进入A装置中的溶液明显多于C装置,此现象还能验证氢氧化钠和氢氧化钙的_____性存在较大差异,所以,实验室吸收二氧化碳用氢氧化钠而不用氢氧化钙。
【答案】铁架台 不变 将导管放入水中,用收握住试管外壁,观察是否有气泡产生,有气泡,说明气密性好 CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ 一 cdef CO2 + Ca(OH)2 == CaCO3 ↓+ H2O m CaCl2溶液能够进入A,溶液中产生白色沉淀 溶解性
【解析】
(1)仪器①的名称为铁架台。
(2)二氧化锰是催化剂,在化学变化中质量和化学性质都不变的质量;检查A装置气密性的方法是:将导管放入水中,用收握住试管外壁,观察是否有气泡产生,有气泡,说明气密性好;
(3)实验室用大理石和稀盐酸制取二氧化碳,反应的化学方程式是CaCO3 + 2HCl == CaCl2 + H2O + CO2↑;装置B中导管只需露出橡胶塞一点即可,故有一处错误;如果要把装置B改装成可控制反应发生和停止的装置,要先取掉带导管的单孔胶塞,再从仪器盒中选择的仪器是cdef。
(4)图C可用于检验二氧化碳,反应方程式是CO2 + Ca(OH)2 == CaCO3 ↓+ H2O,气体从长端进。
(5)①氢氧化钠与二氧化碳反应生成碳酸钠,A中的压强变小,会使CaCl2溶液能够进入A,氯化钙和碳酸钠反应生成碳酸钙沉淀,溶液中产生白色沉淀,故填:CaCl2溶液能够进入A,溶液中产生白色沉淀。
②实验后进入A装置中的溶液明显多于C装置,是因为氢氧化钠的溶解度大于氢氧化钙,吸收的二氧化碳多余,故填:溶解性。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】(1)某研究性学习小组为验证“氨气还原氧化铜”的实验,认真阅资料并做出以下准备。
资料准备:I.氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,溶液呈碱性。
Ⅱ.氨气还原氧化铜的化学反应原理:2NH3+3CuO![]() 3Cu+N2+3H2O。
3Cu+N2+3H2O。
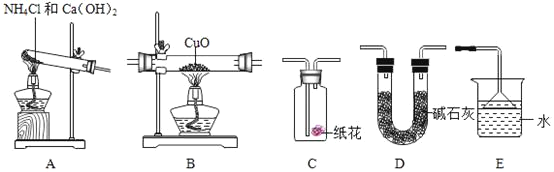
实验准备:
请回答:
①为达成“氨气还原氧化铜”的实验目的,装置A、B、D、E的正确连接顺序_____;(填序号)
②装置A中发生反应的化学方程式_____;
③装置B观察到的现象_____,装置E的作用_____;
④将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变蓝色,原因是_____。
(2)金属镁可与热水反应生成氢氧化镁和氢气,所得溶液呈碱性,可使酚酞溶液显紅色。某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,变为红色,放置在空气中一段时间后,发现溶液的红色褪去了。
①镁与热水反应的化学方程式是_____。
②查阅资料:溶液红色褪去的原因是溶液碱性减弱。
(提出问题)导致溶液碱性减弱的原因是什么?
(假设与分析)
假设1:可能是氢氧化镁与N2或O2发生了反应。
假设2:可能是溶液吸收了空气中的_____。
假设3:可能是氢氧化镁的溶解度随温度的降低而_____。
由碱的性质可知,假设1不成立。
(实验探究)
实验操作 | 实验现象 | 结论 |
(1)取上述红色溶液,保持温度不变,在空气中放置一段时间,观察现象。 | _____ | 假设2成立 |
(2)取上述红色溶液,_____,_____,观察现象。 | 红色褪去 | 假设3成立 |
(拓展延伸)
③将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀。
请解释其原因:_____。
④除上述金属外,根据金属活动性顺序,预测_____也能跟硫酸铜溶液反应产生上述现象(举一例即可)。