题目内容
【题目】科学探究是奇妙的过程,请你一起参与实验探究。
(提出问题)不同的氧化物在氯酸钾制取氧气实验中能否起催化作用
(设计实验)按下表完成实验
实验编号 | 氯酸钾质量 | 氧化物 | 产生气体的体积 | 耗时 |
1 | 0.6g | / | 9.8mL | 480s |
2 | 0.6g | 0.2g二氧化锰 | 67mL | 36.5s |
3 | 0.6g | 0.2g氧化铁 | 67mL | 89.5s |
(1)写出实验2反应的化学方程式_____;
(2)测量实验3中氧气的体积,所需的量筒规格为_____(选填“10”、“50”或“100”)mL;
(3)为证明氧化铁是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ在实验3反应后的混合物中加足量的水溶解,过滤,将滤渣洗涤并干燥,用电子天平称量,质量为0.2g;
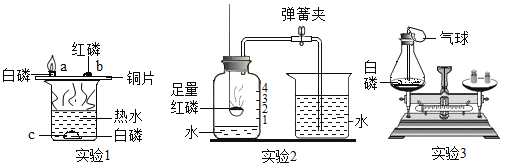
Ⅱ将过量的CO通入滤出的固体,按下图所示装置进行实验,并分析研究。
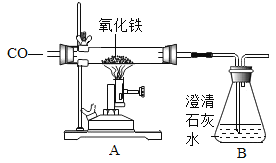
甲同学的实验报告如下:
装置 | 现象 | 结论 |
A | 红色固体全部变黑 | 生成了铁 |
B | ______ | 产生了二氧化碳 |
A处的化学方程式:_____。
(实验结论)以上实验证明氧化铁能作为氯酸钾受热分解的催化剂。两种氧化物相比,_____(选填“二氧化锰”或“氧化铁”)的催化效果好。
(定量计算)若该实验玻璃管中的固体质量减少了0.03克,求:(写出计算过程)
①氧化铁的质量?_____
②生成多少克的铁?_____
(交流反思)上图所示实验装置存在不足之处,理由是_____。
【答案】2KClO3![]() 2KCl+3O2↑ 100 澄清石灰水变浑浊 Fe2O3+3CO
2KCl+3O2↑ 100 澄清石灰水变浑浊 Fe2O3+3CO![]() 2Fe+3CO2 二氧化锰 0.1g 0.07g 没有参加反应的一氧化碳会污染空气
2Fe+3CO2 二氧化锰 0.1g 0.07g 没有参加反应的一氧化碳会污染空气
【解析】
[设计实验]
(1)实验2是氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3![]() 2KCl+3O2↑;故填:2KClO3
2KCl+3O2↑;故填:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(2)量筒使用时,应该采用就近原则,所以测量实验3中氧气的体积为67mL,所需的量筒规格为100mL;故填:100;
(3)二氧化碳和氢氧化钙反应会生成碳酸钙沉淀和水,所以
装置 | 现象 | 结论 |
A | 红色固体全部变黑 | 生成了铁 |
B | 澄清石灰水变浑浊 | 产生了二氧化碳 |
故填:澄清石灰水变浑浊;
A处是氧化铁和一氧化碳在高温条件下生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
故填:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
[实验结论]
从表中的数据可知,在气体条件相同的条件下,用二氧化锰做催化剂时,耗时36.5s;用氧化铁做催化剂时耗时89.5s,所以二氧化锰的催化效果好;
故填:二氧化锰;
[定量计算]
①该实验玻璃管中的固体质量减少了0.03克,即氧化铁中氧元素的质量为0.03g,则氧化铁的质量为:0.03g÷![]() =0.1g;
=0.1g;
②0.1g氧化铁中铁的质量为:0.1g×![]() =0.07g;
=0.07g;
故填:0.1g;0.07g;
[交流反思]
上图所示实验没有尾气处理装置,没有参加反应的一氧化碳会污染空气。
故填:没有参加反应的一氧化碳会污染空气。

 名校课堂系列答案
名校课堂系列答案