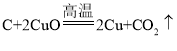题目内容
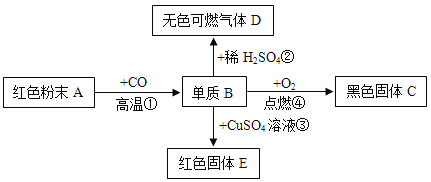
【题目】A、B、C、D、E是初中化学中的五种常见物质。A、B中含有相同的元素,A为暗紫色固体,A在一定的条件下可以生成B。C、D是单质,硫酸铜溶液能与铁丝反应生成单质C;D是密度最小的气体。E俗名双氧水,在一定的条件下可以分解。
(1)请写出物质的化学式。A:_____ C:_____ E:_____。
(2)写出化学方程式。
①硫酸铜溶液与铁丝反应:_____。
②A在一定条件下生成B:_____。
③E在一定条件下分解:_____。
【答案】KMnO4 Cu H2O2 Fe+CuSO4=FeSO4+Cu 2KMnO4![]() K2MnO4+MnO2+O2↑ 2H2O2
K2MnO4+MnO2+O2↑ 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
【解析】
A、B、C、D、E是初中化学中的五种常见物质,硫酸铜溶液能与铁丝反应生成单质C,铁与硫酸铜溶液生成硫酸亚铁和铜,所以C是铜;D是密度最小的气体,所以D是氢气;E俗名双氧水,在一定的条件下可以分解,所以E是过氧化氢溶液;A、B中含有相同的元素,A为暗紫色固体,A在一定的条件下可以生成B。高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,所以A是高锰酸钾,B是锰酸钾。经过验证,推导正确。
根据以上分析可知:
(1)A是KMnO4,C是Cu,E是H2O2;
(2)①硫酸铜溶液与铁丝的反应是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;
②A在一定条件下生成B的反应是高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为::2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
③E在一定条件下分解的反应是过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】科学探究是奇妙的过程,请你一起参与实验探究。
(提出问题)不同的氧化物在氯酸钾制取氧气实验中能否起催化作用
(设计实验)按下表完成实验
实验编号 | 氯酸钾质量 | 氧化物 | 产生气体的体积 | 耗时 |
1 | 0.6g | / | 9.8mL | 480s |
2 | 0.6g | 0.2g二氧化锰 | 67mL | 36.5s |
3 | 0.6g | 0.2g氧化铁 | 67mL | 89.5s |
(1)写出实验2反应的化学方程式_____;
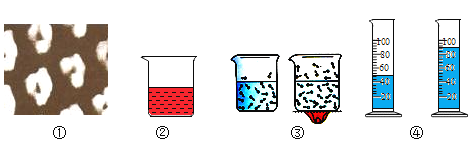
(2)测量实验3中氧气的体积,所需的量筒规格为_____(选填“10”、“50”或“100”)mL;
(3)为证明氧化铁是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ在实验3反应后的混合物中加足量的水溶解,过滤,将滤渣洗涤并干燥,用电子天平称量,质量为0.2g;
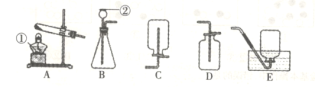
Ⅱ将过量的CO通入滤出的固体,按下图所示装置进行实验,并分析研究。
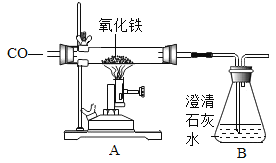
甲同学的实验报告如下:
装置 | 现象 | 结论 |
A | 红色固体全部变黑 | 生成了铁 |
B | ______ | 产生了二氧化碳 |
A处的化学方程式:_____。
(实验结论)以上实验证明氧化铁能作为氯酸钾受热分解的催化剂。两种氧化物相比,_____(选填“二氧化锰”或“氧化铁”)的催化效果好。
(定量计算)若该实验玻璃管中的固体质量减少了0.03克,求:(写出计算过程)
①氧化铁的质量?_____
②生成多少克的铁?_____
(交流反思)上图所示实验装置存在不足之处,理由是_____。