题目内容
【题目】氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于酸)为原料制备高纯氧化镁的实验流程如下:
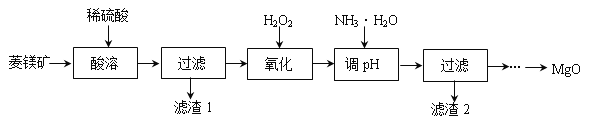
(1)酸溶之前要将矿石粉碎的目的是 。稀硫酸需要过量的目的是 。酸溶步骤中碳酸镁溶解的反应方程式为 。
(2)已知Mg2+、Fe2+和Fe3+在溶液中遇到氨水均可以转化成难溶性碱沉淀,开始沉淀和沉淀完全的pH如下表:
Mg2+ | Fe2+ | Fe3+ | |
开始沉淀 | 9.4 | 7.9 | 2.7 |
沉淀完全 | 12.4 | 9.6 | 3.7 |
流程“氧化”一步中H2O2的作用是将溶液中的Fe2+转化成Fe3+,不能直接沉淀Fe2+的原因是 。
(3)加氨水调节溶液的PH范围为 。
(4)滤渣2的化学式是 。
【答案】(1)增大矿石与酸的接触面积,使反应更快更充分 使MgCO3和FeCO3完全反应
MgCO3+H2SO4= MgSO4+H2O+CO2↑(2)防止Mg2+沉淀出来(3)3.7~9.4(4)Fe(OH)3
【解析】
试题分析:酸溶之前要将矿石粉碎的目的是增大矿石与酸的接触面积,使反应更快更充分。稀硫酸需要过量的目的是使MgCO3和FeCO3完全反应。酸溶步骤中碳酸镁溶解的反应方程式为MgCO3+H2SO4= MgSO4+H2O+CO2↑,流程“氧化”一步中H2O2的作用是将溶液中的Fe2+转化成Fe3+,不能直接沉淀Fe2+的原因是防止Mg2+沉淀出来。加氨水调节溶液的PH范围为3.7~9.4。滤渣2的化学式是Fe(OH)3。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目