题目内容
【题目】某班同学为验证酸的化学通性,做了五组实验。分析并回答问题。
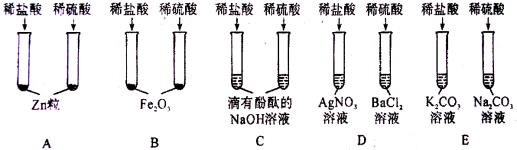
(1)A组试管中都产生H2。若要制得较纯的H2,选稀硫酸而不选盐酸的原因是 。
(2)C组试管中药品滴加至一定程度实验现象相同,该现象是 。
(3)写出D组任一试管中发生反应的化学方程式 。
(4)上述五组实验中没有体现酸的通性的是 (填序号)。
【答案】(1)盐酸有挥发性或盐酸会挥发出氯化氢气体或制得的氢气中混有氯化氢气体 。
(2)红色溶液退为无色
(3)HCl+AgNO3 = AgCl↓(白色)+HNO3或H2SO4+BaCl2 = BaSO4↓(白色)+2HCl。
(4)D
【解析】
试题分析:(1)盐酸具有挥发性,挥发出氯化氢气体,制得的氢气中混有氯化氢气体,不纯净.
(2)C组试管中药品滴加,酸与碱发生中和反应,消耗了NaOH溶液,现象为红色溶液退为无色
(3)氯化钡与硫酸反应生成硫酸钡和盐酸,H2SO4+BaCl2 = BaSO4↓+2HCl
(4)酸能与酸碱指示剂、活泼金属、金属氧化物、碱、盐等反应,ABCE分别能体现酸能与活泼金属、金属氧化物、碱、碳酸盐等反应;D中盐酸只能与硝酸银溶液反应,故五组实验中没有体现酸的通性的是D,

【题目】氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于酸)为原料制备高纯氧化镁的实验流程如下:
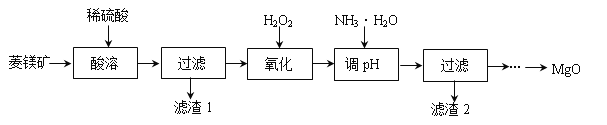
(1)酸溶之前要将矿石粉碎的目的是 。稀硫酸需要过量的目的是 。酸溶步骤中碳酸镁溶解的反应方程式为 。
(2)已知Mg2+、Fe2+和Fe3+在溶液中遇到氨水均可以转化成难溶性碱沉淀,开始沉淀和沉淀完全的pH如下表:
Mg2+ | Fe2+ | Fe3+ | |
开始沉淀 | 9.4 | 7.9 | 2.7 |
沉淀完全 | 12.4 | 9.6 | 3.7 |
流程“氧化”一步中H2O2的作用是将溶液中的Fe2+转化成Fe3+,不能直接沉淀Fe2+的原因是 。
(3)加氨水调节溶液的PH范围为 。
(4)滤渣2的化学式是 。