题目内容
【题目】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)地壳中含量居第一位的金属元素是______(填元素符号)。
(2)日常使用的金属材料多数属于合金,与组成合金的纯金属相比,合金的优点一般有______(填序号)
①强度更低;②硬度更高;③熔点低;④抗腐蚀性更好
(3)某化学兴趣小组的学生发现金属R不在初中学到的金属活动性顺序表中,该小组为了了解R与常见金属铝、铜的金属活动性顺序,进行如下探究活动;
(作出猜想)他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R;
猜想二______
猜想三:R>Al>Cu
(查阅资料)R是一种银白色的金属,在R的盐溶液中只有+2价,R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜:硫酸铝、氧化铝、硝酸铝的溶液均为无色。
(实验探究)为了探究哪一种猜想成立,甲、乙、丙三名同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究。
猜想 | 主要操作 | 主要现象 | 实验结论 |
猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一 ______ (填“成立”或“不成立”) |
猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立。 R与稀硫酸反应的化学方程式为______ |
猜想三 | ______ | 无明显现象 | 猜想三成立 |
(交流反思)
究竟哪种猜想成立?三名同学经讨论交流发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误。于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后溶液的颜色______;进而确认猜想三不成立,猜想二成立。
(4)为了测定铜锌合金样品中锌的质量称取样品20g于烧杯中,向其中加入50g稀硫酸至恰好完全反应反应后烧杯中物质的总质量为69.8g。请计算:样品中锌的质量。______
【答案】Al ②③④ Al>R>Cu 不成立 R+H2SO4=RSO4+H2↑ 将铝丝插入到RSO4溶液中 消失 6.5g
【解析】
(1)根据金属的含量进行解答;
(2)根据合金的特性进行解答;
(3)根据给出的信息和结论结合操作中要点进行分析和解答;
(4)根据质量守恒定律可知,过程中质量的减少是因为生成了氢气,所以可以求算氢气的质量,根据氢气的质量和对应的化学方程式求算样品中锌的质量。
(1)地壳中含量居第一位的金属元素是铝,对应的元素符号为Al;
(2)日常使用的金属村料多数属于合金,与组成合金的纯金属相比,合金的优点一般有硬度更高、熔点低、抗腐蚀性更好等;
(3)考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:猜想一:Al>Cu>R;猜想二:Al>R>Cu;猜想三:R>Al>Cu.(最前,中间和最后。相当于插空)
R丝表面覆盖了一层红色的物质,说明R比铜活泼,猜想一不成立;
根据R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色,证明R和硫酸反应,由于提示在R的盐溶液中只有+2价,所以对应的化学方程式为:R+H2SO4=RSO4+H2↑;
由于实验中结论为猜想三成立,即R比铝活泼,而对应现象是无明显现象,说明是将铝丝插入到RSO4溶液中,这样无明显现象才能说明猜想三成立;
由于最终结论是猜想三不成立,而猜想二成立,所以应该是打磨过的铝丝插入RSO4溶液中,而颜色消失,证明铝比R活泼,即猜想二成立;
(4)根据质量守恒定律可得,生成的氢气的质量为20g+50g-69.8g=0.2g;
设样品中锌的质量为x,
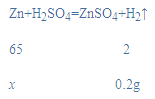
![]()
x=6.5g。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】下列反应中,属于置换反应的是
A. 2Al2O3![]() 4Al+3O2↑ B. C2H5OH+302
4Al+3O2↑ B. C2H5OH+302![]() 2CO2+3H20
2CO2+3H20
C. 2Mg+CO2![]() 2MgO+C D. AgNO3+NaCl=NaNO3+AgCl↓
2MgO+C D. AgNO3+NaCl=NaNO3+AgCl↓
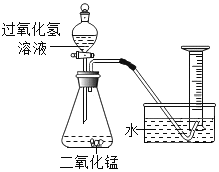
【题目】过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
Ⅰ.不稳定性
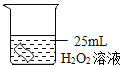
(1)如图所示进行实验,过氧化氢分解的化学方程式为______,产生3.2gO2时分解的过氧化氢的质量为______g。
(2)能用排水法收集O2的原因是______。
(3)探究温度对过氧化氢分解速率的影响
同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度% | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40min | 40min | 40min |
由此得出的结论是______。
Ⅱ.腐蚀性
(査阅资料)H2O2溶液有腐蚀性。
(进行实验)
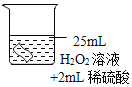
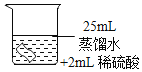
将铜片分别浸泡在3种溶液中进行实验,如下表。
编号 | ① | ② | ③ |
实验 |
|
|
|
一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
(解释与结论)
(4)实验①的作用是______。
(5)铜片被腐蚀的反应如下,补全该反应的化学方程式:Cu+H2O2+H2SO4=CuSO4+______。
(反思交流)
(6)某同学提出,实验②中,除发生(5)的反应外。还发生了一个反应导致有细小气泡产生,该反应的反应物为______。