题目内容
某化工厂排放的废水中含有一定量的氢氧化钾,为了回收利用,欲用2%的稀盐酸测定废水中的氢氧化钾含量(废水中其它杂质不与盐酸反应)。试计算:
(1)用10克30%的浓盐酸配制成2%的稀盐酸,需加水多少克?
(2)取40克废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸18.25克,求废水中氢氧化钾的质量分数?
(1)140g; (2)1%
解析试题分析:(1)根据溶液稀释前后,溶质的质量不变,据此结合题意进行分析解答。
(2)氢氧化钾与稀盐酸反应生成氯化钾和水,根据题意,取40克废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸18.25克,据此由反应的化学方程式计算出废水中氢氧化钾的质量,进而计算出废水中氢氧化钾的质量分数。
解:(1)设要加水的质量为x,根据溶液稀释前后,溶质的质量不变,则
10g×30%=(10g+x)×2%
解得x=140g
(2)18.25g稀盐酸中含溶质的质量为18.25g×2%=0.365g
设设参加反应的氢氧化钾的质量为y,则
HCl+KOH=KCl+H2O
36.5 56
0.365g y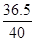 =
=
解得y=0.4g
废水中氢氧化钾的质量分数为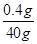 ×100%=1%
×100%=1%
答:(1)140g;(2)废水中氢氧化钾的质量分数为1%
考点:考查根据化学反应方程式的计算;用水稀释改变浓度的方法;有关溶质质量分数的简单计算

练习册系列答案
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目