题目内容
【题目】蚊虫叮咬分泌出乙酸刺激皮肤,某兴趣小组对乙酸进行如下的探究:
【查阅资料】:甲酸,又称乙酸,具有酸的通性,甲酸的熔点是8.6℃,受热能分解生成两种物质。
实验探究一:验证甲酸的酸性,完成实验记录。
操作 | 实验现象 | 原理或解释 | |
取甲酸溶于水 | 滴加紫色石蕊 | 溶液变成红色 | 溶液中含有_____填离子符号) |
加适量的锌粒 | 观察到有气泡产生 | 锌粒与甲酸生成了Zn(HCOO)2和一种气体,写出该反应的方程式__________ | |
加氢氧化镁粉末 | 观察到_____ | 甲酸可以与碱反应 |
实验探究二:探究甲酸分解的产物。
【提出猜想】:实验小组对甲酸的分解产物提出了猜想:
猜想1:H2和CO2;猜想二:CO和H2O。
同学们提出以上猜想的依据是:__________________________
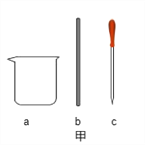
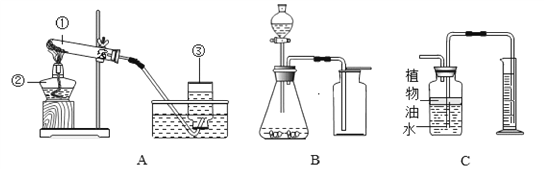
【设计实验】根据资料,小组同学从下图装置中选择装置图_______(填“甲”或‘乙’)对甲酸进行加热。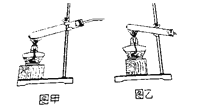
【交流与拓展】资料表明,甲酸的分解产物不同,猜想一与猜想二均成立。据此小林对甲酸的分解产物又提出新猜想-----猜想3:H2O和CO2;猜想四:CO与H2,同学们讨论后认为无需进行实验就知道猜想三和猜想四是错误的,理由是:_____________
【答案】 H+, Zn+2HCOOH=Zn(HCOO)2+H2↑ , 粉末溶解, 甲酸中有碳氢氧元素, 乙, 二氧化碳溶于水,不符合质量守恒定律
【解析】【实验探究一】能使石蕊试液变红色的溶液显酸性,溶液中含有H+;锌粒与甲酸生成了Zn(HCOO)2和一种气体,该反应的方程式为:Zn+2HCOOH=Zn(HCOO)2+H2↑;甲酸可以与碱反应,所以氢氧化镁粉末溶解;【实验探究二】根据蚁酸中含有碳、氢、氧元素,根据质量守恒定律,可推测出生成物中可能含有水、一氧化碳、二氧化碳;【设计实验】常温下,甲酸为固体,加热甲酸时,试管口应略向下倾斜;【拓展延伸】根据质量守恒定律,若生成物为水和二氧化碳,二氧化碳溶于水,不符合质量守恒定律。

【题目】下列事实解释不正确的是()
选项 | 事实 | 解释 |
A | NaOH 和 |
|
B | 金刚石、石墨高温下都可以燃烧 | 它们都是有碳原子构成的 |
C | 给装满水的纸杯加热,开始时纸杯完好无损 | 温度没有达到纸的着火点 |
D | 酒精灯不用时,需用灯帽盖好 | 防止酒精挥发到空气中 |
A. A B. B C. C D. D