题目内容
【题目】化学是一门以实验为基础的科学,请你和化学小组同学一起完成下列实验。
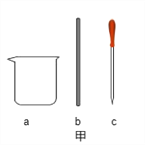

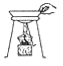
实验一:现提供图甲的仪器
用浓HCl(溶质质量分数为37%,密度为1.18g/mL)配制200g 10%的稀HCl。
⑴ 配制的主要步骤为:计算、______ 、混匀。
⑵ 设需要浓HCl的体积为V,请列出V的计算式:______(不必计算结果);配制过程中还需要的仪器有______ 。
实验二:现提供图乙的仪器
⑴若实验室要用同一装置制取并收集O2和CO2,最好选择______(填字母序号),写出该装置制取CO2 的化学方程式__________________________________ 。
⑵实验室用A装置和一种纯净物也制得了O2 ,该反应的化学方程式为__________。若试管破裂,则原因可能是__________________________________。
⑶某些大理石含有少量硫化物,使制得CO2 中混有H2S气体。欲获取纯净、干燥的CO2 ,需要对发生装置中产生的气体进行除杂,实验装置如图:
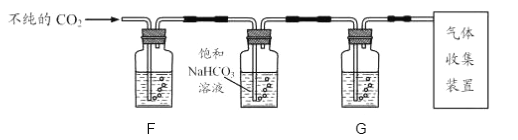
查阅资料:Ⅰ.H2S能与NaOH等碱溶液、CuSO4溶液反应。
Ⅱ. CO2 中混有的HCl气体可用饱和NaHCO3溶液吸收。
①装置F中所盛试剂应选用_______(填字母)。
A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液
②装置G的作用是_________。
【答案】 溶解 V=200g×10%/1.18g.mL-1× 37% 量筒 BD CaCO3 + 2HCl = CaCl2 + CO2↑ 2KMnO4![]() K2MnO4+MnO2+O2↑ 集中加热前没有均匀受热 D 干燥二氧化碳气体
K2MnO4+MnO2+O2↑ 集中加热前没有均匀受热 D 干燥二氧化碳气体
【解析】实验一:⑴用浓溶液配制稀溶液的主要步骤为:计算、溶解、混匀。⑵稀释前后溶质质量相等,V=![]() ,配制过程中需要的仪器有烧杯、玻璃棒、量筒、滴管。实验二:⑴实验室用固体石灰石与稀盐酸制取二氧化碳气体,固液常温反应制取气体选择发生装置B,收集二氧化碳只能用向上排空气法,所以实验室要用同一装置制取并收集O2和CO2,选择的装置是BD,制取CO2 的化学方程式是:CaCO3 + 2HCl = CaCl2 + CO2↑。⑵实验室用A装置和一种纯净物也制得了O2 ,则是用高锰酸钾制取氧气,反应的化学方程式为:2KMnO4
,配制过程中需要的仪器有烧杯、玻璃棒、量筒、滴管。实验二:⑴实验室用固体石灰石与稀盐酸制取二氧化碳气体,固液常温反应制取气体选择发生装置B,收集二氧化碳只能用向上排空气法,所以实验室要用同一装置制取并收集O2和CO2,选择的装置是BD,制取CO2 的化学方程式是:CaCO3 + 2HCl = CaCl2 + CO2↑。⑵实验室用A装置和一种纯净物也制得了O2 ,则是用高锰酸钾制取氧气,反应的化学方程式为:2KMnO4 ![]() K2MnO4 + MnO2 + O2↑,若试管破裂,则原因可能是集中加热前没有均匀受热。⑶①根据提供的信息知道,H2S能与NaOH等碱溶液、CuSO4溶液反应,但二氧化碳能与NaOH等碱溶液反应,所以装置F中所盛试剂应选用CuSO4溶液。②装置G中盛放浓硫酸,作用是干燥二氧化碳气体。
K2MnO4 + MnO2 + O2↑,若试管破裂,则原因可能是集中加热前没有均匀受热。⑶①根据提供的信息知道,H2S能与NaOH等碱溶液、CuSO4溶液反应,但二氧化碳能与NaOH等碱溶液反应,所以装置F中所盛试剂应选用CuSO4溶液。②装置G中盛放浓硫酸,作用是干燥二氧化碳气体。

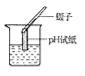
【题目】某学习小组在探究碳酸钠的化学性质时,做了下面所示三个实验.
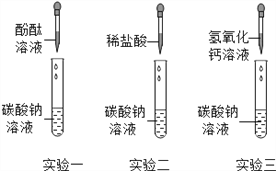
(1)实验一:探究碳酸钠溶液的酸碱性。观察到试管中溶液变为红色,可得出结论是 ________________________
实验二:探究碳酸钠与稀盐酸的反应.试管中产生大量气泡,该反应化学方程式为 _______________________。
实验三:探究碳酸钠与氢氧化钙溶液的反应.试管中产生白色沉淀,该白色沉淀为 ________
(2)小组同学将实验三试管内液体进行过滤,对滤液中溶质成分展开了探究.
【提出问题】滤液中溶质成分是什么?
【猜想】
猜想一:滤液中溶质是氢氧化钠;
猜想二:滤液中溶质是氢氧化钠、氢氧化钙和碳酸钠;
猜想三:滤液中溶质是氢氧化钠、氢氧化钙;
猜想四:滤液中溶质是______________
【讨论】大家一致认为猜想二不成立,理由是 ___________________________________。
【实验验证】
小组同学通过以下实验验证了猜想三成立,请你完成实验报告.
实验步骤 | 实验现象 | 实验结论 |
取实验三少量滤液与试管中,通入二氧化碳气体 | _______________ | 猜想三成立 |
(3)实验结束,同学对废液进行处理,将实验一、实验二溶液倒入同一洁净烧杯,得到无色溶液,则实验二试管中溶液含有溶质为 ________________。
【题目】某气体可能是氢气、一氧化碳、二氧化碳、水蒸气、氯化氢气体中的一种或几种组成,为确定其成分,某兴趣小组设计了如下实验(已知无水硫酸铜遇水变蓝)

气体通过有关装置时观察到的现象如下(假设每步反应均完全进行):
装置编号 | A | B | C | D | E |
试剂 | 硝酸银溶液 | 澄清石灰水 | 氧化铜粉末 | 澄清石灰水 | 无水硫酸铜 |
现象 | 白色沉淀 | 变浑浊 | 变红色 | 无明显变化 | 变蓝色 |
下列说法中错误的是
A. 该气体中一定有氯化氢气体、氢气、二氧化碳
B. 该气体中一定不含一氧化碳
C. 若将装置D、E位置颠倒,可以判断水蒸气是否存在
D. 若将装置A、B位置颠倒,只影响氯化氢气体的检验
【题目】蚊虫叮咬分泌出乙酸刺激皮肤,某兴趣小组对乙酸进行如下的探究:
【查阅资料】:甲酸,又称乙酸,具有酸的通性,甲酸的熔点是8.6℃,受热能分解生成两种物质。
实验探究一:验证甲酸的酸性,完成实验记录。
操作 | 实验现象 | 原理或解释 | |
取甲酸溶于水 | 滴加紫色石蕊 | 溶液变成红色 | 溶液中含有_____填离子符号) |
加适量的锌粒 | 观察到有气泡产生 | 锌粒与甲酸生成了Zn(HCOO)2和一种气体,写出该反应的方程式__________ | |
加氢氧化镁粉末 | 观察到_____ | 甲酸可以与碱反应 |
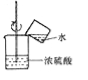
实验探究二:探究甲酸分解的产物。
【提出猜想】:实验小组对甲酸的分解产物提出了猜想:
猜想1:H2和CO2;猜想二:CO和H2O。
同学们提出以上猜想的依据是:__________________________
【设计实验】根据资料,小组同学从下图装置中选择装置图_______(填“甲”或‘乙’)对甲酸进行加热。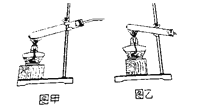
【交流与拓展】资料表明,甲酸的分解产物不同,猜想一与猜想二均成立。据此小林对甲酸的分解产物又提出新猜想-----猜想3:H2O和CO2;猜想四:CO与H2,同学们讨论后认为无需进行实验就知道猜想三和猜想四是错误的,理由是:_____________