题目内容
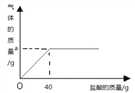
【题目】草木灰的主要成分是碳酸钾。某化学兴趣小组取100g草木灰样品于烧杯中,不断滴入稀盐酸,当烧杯中的残余混合物质量为137.8g时,充分反应。反应过程放出的气体质量与加入盐酸的关系曲线如图表示。(假设草木灰的其他成分不与酸反应)
请计算回答:
(1)图中纵坐标上a点数值:a=__________g;放出气体的物质的量为__________ mol。
(2)草木灰样品中碳酸钾的质量分数为________________(要求写出计算过程)。
【答案】 2.2 0.05 6.9%
【解析】(1)根据质量守恒定律,a=100g+40g-137.8g=2.2g,生成的气体是二氧化碳气体,二氧化碳的物质的量为:![]() =0.05mol
=0.05mol
(2)设草木灰样品中碳酸钾的质量为x。
K2CO3 + 2HCl == 2KCl + H2O + CO2↑
138 44
x 2.2g
![]() =
=![]() ,解得x=6.9g
,解得x=6.9g
草木灰样品中碳酸钾的质量分数为:![]() ×100%=6.9%
×100%=6.9%

【题目】蚊虫叮咬分泌出乙酸刺激皮肤,某兴趣小组对乙酸进行如下的探究:
【查阅资料】:甲酸,又称乙酸,具有酸的通性,甲酸的熔点是8.6℃,受热能分解生成两种物质。
实验探究一:验证甲酸的酸性,完成实验记录。
操作 | 实验现象 | 原理或解释 | |
取甲酸溶于水 | 滴加紫色石蕊 | 溶液变成红色 | 溶液中含有_____填离子符号) |
加适量的锌粒 | 观察到有气泡产生 | 锌粒与甲酸生成了Zn(HCOO)2和一种气体,写出该反应的方程式__________ | |
加氢氧化镁粉末 | 观察到_____ | 甲酸可以与碱反应 |
实验探究二:探究甲酸分解的产物。
【提出猜想】:实验小组对甲酸的分解产物提出了猜想:
猜想1:H2和CO2;猜想二:CO和H2O。
同学们提出以上猜想的依据是:__________________________
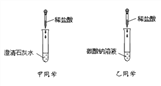
【设计实验】根据资料,小组同学从下图装置中选择装置图_______(填“甲”或‘乙’)对甲酸进行加热。
【交流与拓展】资料表明,甲酸的分解产物不同,猜想一与猜想二均成立。据此小林对甲酸的分解产物又提出新猜想-----猜想3:H2O和CO2;猜想四:CO与H2,同学们讨论后认为无需进行实验就知道猜想三和猜想四是错误的,理由是:_____________