题目内容
【题目】近年来,多次发生煤矿瓦斯燥炸事件。瓦斯已成为导致我国煤矿特大恶性事的“头号杀手”。
(1)瓦斯的主要成分是甲烷,在空气中完全燃烧的化学方程式为_____。
(2)矿井下瓦斯爆炸事故发生后,专家提出了注入液氮灭火的方案。液氮可用于矿井灭火的原因除了液氮汽化使温度降低外,还因为_____。
(3)检测人员抽取了某矿井气体样品X,X中可能含有一氧化碳、二氧化碳和甲烷三种气体中的一种或多种。为了确认气体X的成分,某同学设计了如下探究装置(假设每步都充分反应或吸收):
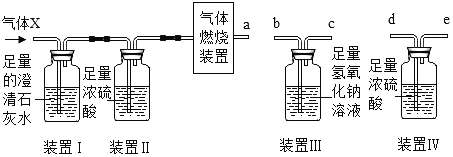
①为保证实验的准确性,气体燃烧装置后应该连接的导管序号是a→_____。
②若装置I中无明显变化,装置Ⅲ增重3.6g,装置Ⅳ增重2.7g,则可判断气体样品X中一定含有的气体是_____(填化学式)。
【答案】CH4+2O2![]() CO2+2H2O 不助燃,不可燃 d→e→b→c 甲烷和一氧化碳
CO2+2H2O 不助燃,不可燃 d→e→b→c 甲烷和一氧化碳
【解析】
(1)甲烷和氧气在点燃的条件下生成水和二氧化碳,化学方程式为:CH4+2O2![]() CO2+2H2O;
CO2+2H2O;
(2)液氮可用于矿井灭火的原因除了液氮汽化使温度降低外,还因为不助燃,不可燃;
(3)①甲烷燃烧产生二氧化碳和水,二氧化碳和水的检验应该先检验水再检验二氧化碳,否则会影响水的检验,因此先通过浓硫酸再通过氢氧化钠溶液,并且要长管进,短管出,气体燃烧装置后应该连接的导管序号是a→d→e→b→c;
②若装置I中无明显变化,说明没有二氧化碳;装置Ⅲ增重3.6g,说明生成了3.6g二氧化碳,其中碳元素的质量为:3.6g×![]() ×100%=0.98g;装置Ⅳ增重2.7g,说明生成了2.7g水,其中氢元素的质量为:2.7g×
×100%=0.98g;装置Ⅳ增重2.7g,说明生成了2.7g水,其中氢元素的质量为:2.7g×![]() ×100%=0.3g,因此碳元素和氢元素的质量比为98:30,而甲烷中碳元素和氢元素的质量比为12:4=3:1<98:30,所以气体样品X中一定含有的气体是甲烷和一氧化碳。
×100%=0.3g,因此碳元素和氢元素的质量比为98:30,而甲烷中碳元素和氢元素的质量比为12:4=3:1<98:30,所以气体样品X中一定含有的气体是甲烷和一氧化碳。
故答案为:(1)CH4+2O2![]() CO2+2H2O;(2)不助燃,不可燃;(3)①d→e→b→c;②甲烷和一氧化碳。
CO2+2H2O;(2)不助燃,不可燃;(3)①d→e→b→c;②甲烷和一氧化碳。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】某化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究。

(提出问题)这是一瓶什么溶液?
(猜想与假设)
小红同学的猜想是Na2SO3溶液,小明同学的猜想是Na2SO4溶液,你的猜想是_____溶液(填一种即可)。
(查阅资料)
①BaSO3一种不溶于水的白色沉淀,但溶于稀盐酸,能与稀盐酸发生反应。
②硝酸具有强氧化性,能将BaSO3氧化成BaSO4
③Na2SO3与稀盐酸反应生成SO2,SO2能使澄清石灰水变浑浊,也能使品红溶液褪色。
(进行实验)
(1)小红同学取适量的该溶液于试管中,滴加稀盐酸,产生无色气体,她认为自己的猜想成立,而小明同学认为她的结论不合理,原因是_____。
(2)小明同学为了验证自己的猜想,做了如下实验:
取适量的该溶液于试管中,先滴加足量的BaCl2溶液,再滴加过量硝酸,现象为_____,小明同学认为自己的猜想成立。
(3)小马同学对小明同学的结论也提出了质疑,他认为滴加BaCl2溶液和稀硝酸,Na2SO3也会产生同样的现象,为了证明自己的观点,做了如下实验:
步骤 | 操作 | 实验现象 | 实验结论 |
步骤1 | 取少量该溶液于试管中,滴加足量的BaCl2溶液 | _____ | 无 |
步骤2 | 向步骤1的试管中滴加足量的稀盐酸 | _____ | 此溶液不是Na2SO4 |
步骤3 | 将步骤2中产生的气体通入品红溶液中 | 品红溶液褪色 | _____ |
写出小马同学实验过程中的化学方程式_____,_____。