题目内容
【题目】生活中常见物质的性质、制法等是化学研究的重要内容.
(1)化合反应发生后,生成物肯定不会是_____(填“单质”或“化合物”).
(2)①钠与水反应生成氢氧化钠和氢气,化学方程式为_____.
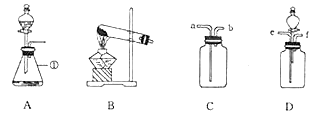
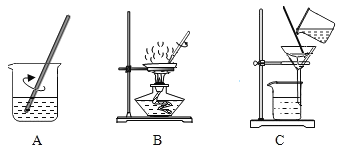
②下列实验仪器中不能用于加热的是_____(填字母).
a 烧杯 b 量筒 c 试管 d 蒸发皿
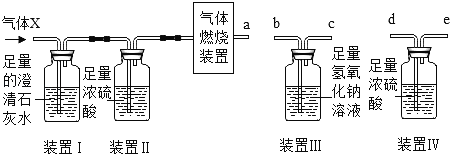
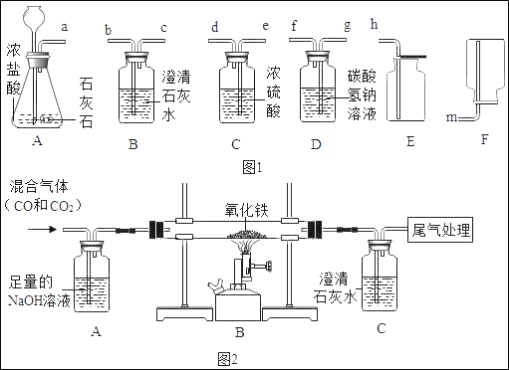
(3)某化学小组选用(如图1)装置和药品进行探究实验.
①A中反应的化学方程式为_____.
②若用以上装置制取并收集一瓶纯净、干燥的二氧化碳气体,请你选择合适的装置并写出导管口连接的顺序_____.
(4)如图2装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物.
①B装置玻璃管里可观察到的现象是_____.
②C装置中反应的化学方程式为_____.
(5)工业上可利用“铝热反应”焊接刚轨、冶炼难溶金属等,其原理是在高温下用铝将某些金属从其氧化物中置换出来.若用铝与四氧化三铁反应来制取25.2kg铁,理论上需要消耗铝的质量是多少_____?
【答案】单质 2Na+2H2O=2NaOH+H2↑ b CaCO3+2HCl═CaCl2+H2O+CO2↑ agfedh 固体由红色变为黑色 CO2+Ca(OH)2=CaCO3↓+H2O 10.8kg
【解析】
(1)化合反应是两种或者两种以上物质生成一种,所以元素不可能是一种,因此生成物不能是单质;
(2)①钠与水反应生成氢氧化钠和氧气,对应的化学方程式为2Na+2H2O=2NaOH+H2↑。
②给定的仪器中量筒不可以加热也不能盛放热的液体。
(3)①A中是碳酸钙和浓盐酸反应生成了氯化钙和二氧化碳以及水,对应的化学方程式为 CaCO3+2HCl═CaCl2+H2O+CO2↑;
②由于使用了浓盐酸,所以导致生成的二氧化碳混有HCl,同时含有水蒸气,吸收HCl应该使用饱和的碳酸氢钠溶液,除去水蒸气用浓硫酸,洗气瓶应该是长进短出,最后用向上排空气法收集,所以应该是 agfedh.
(4)①B装置玻璃管里一氧化碳和氧化铁反应生成二氧化碳和铁,可观察到的现象是固体由红色变为黑色。
②C装置中反应的化学方程式为 CO2+Ca(OH)2=CaCO3↓+H2O.
(5)解:设需要的铝的质量为x ,

![]()
x=10.8kg
答:需要的铝的质量为10.8kg。

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案