��Ŀ����
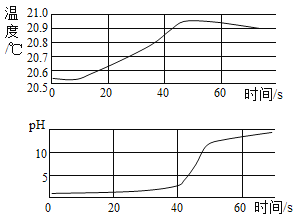
����Ŀ��������������άϵ��Ҫˮ��������ճ������ũҵ�����벻��ˮ��ˮ����õ��ܼ���A��B�������ʵ��ܽ��������ͼ1��ʾ��20��ʱ����A��B���ֹ����50g���ֱ���뵽ʢ��100gˮ���ձ��У���ֽ����������ͼ2��ʾ�����µ�50��ʱ��A��B���ֹ�����ˮ�е��ܽ������ͼ3��ʾ����A��B�����ʾ������ᾧˮ��

��ش��������⣺
��1����20�浽50��ı仯�����У�һֱ���ڱ���״̬����_____���A����B��������Һ��
��2��ͼ1���ܱ�ʾA�����ܽ�����¶ȱ仯��������_____����ס����ҡ�����
��3��ͼ1��P��ĺ���_____��
��4��ͼ3��A��Һ��������������_____������ȷ��0.1%��
���𰸡�B �� 20��ʱ��A��B���ʵ��ܽ����� 33.3%
��������
��1����20�浽50��ı仯�����У�һֱ���ڱ���״̬����B��Һ����ΪB���ձ���һֱ��ʣ��Ĺ��壻���B��
��2��20��ʱ����A��B���ֹ����50g���ֱ���뵽ʢ��100gˮ���ձ��У���ֽ����������ͼ2��ʾ�����µ�50��ʱ��A��B���ֹ�����ˮ�е��ܽ������ͼ3��ʾ��B���ʵĹ�������A���ʵĹ�����٣�˵��A���ʵ��ܽ�����¶ȵ����߶�����B�����෴�����Լ���A���ʵ��ܽ�����ߣ�����B���ʵ��ܽ�����ߡ�����ף�
��3�������ʾ���ʵ��ܽ����ȣ�ͼ1��P��ĺ����ǣ�20��ʱ��A��B���ʵ��ܽ����ȣ����20��ʱ��A��B���ʵ��ܽ����ȣ�
��4��ͼ3��A��Һ��50g������ȫ�ܽ⣬�ܼ�������Ϊ100g����������������Ϊ��![]() �����33.3%��
�����33.3%��

 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д� ����ѧ��ţ��Ӣ��ϵ�д�
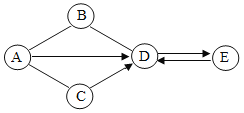
����ѧ��ţ��Ӣ��ϵ�д�����Ŀ��ij��ͬѧΪ��֤̼���ƵĻ�ѧ���ʣ���ʢ��̼���Ƶ��Թ��м���һ������ϡ���ᣬѸ���ô������ܵ����������Թܿڣ�����������һ��ͨ��ʢ�г���ʯ��ˮ���Թ��У���ͼ��ʾ������ش��������⣺
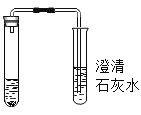
��1���Ҳ��Թ��г���ʯ��ˮ����ǣ�д���÷�Ӧ�Ļ�ѧ����ʽ_____��
��2��ʵ���������֧�Թ��е��������ʵ���ͬһ����Һ���У���ַ�Ӧ��õ�������Һ��ͬѧ�ǶԷ�Һ�����ʵijɷֽ�������̽�������Զ�����̼��Ӱ�죩��
��������⣩
��Һ�����ʵijɷ���ʲô��
���������룩
����һ��CaCl2��NaCl��HCl
�������CaCl2��NaCl��Na2CO3
��������_____��
���������ۣ�
�������ۣ�ͬѧ��һ����Ϊ����_____�Ǵ���ġ�
�����ʵ�飩�����ʵ�鱨��
ʵ�鲽�� | ʵ������ | ʵ����� |
ȡ������Һ���Թ��У�����_____�� | _____�� | ����һ���� |
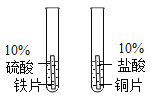
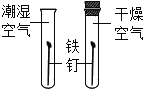
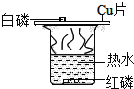
����Ŀ��С��ͬѧ����ϰ�������Ļ�ѧ���ʡ�ʵ�����ʱ,���ּ�֧�Թ������ݲ����������п�����,��������С��ͬѧһ�������������̽����
��������⣩�������ᷴӦ�Ŀ�������Щ����Ӱ����?
����������裩����һ:���������Ũ���й�;
�����:����������������й�;
������:�������������״�йء�
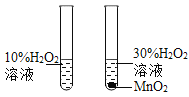
����Ʋ�����ʵ�� ��Ϊ����֤����,С����С�������ͼ��ʾװ�ý���ʵ�顣
��� | �����Ũ��(��ȡ20 mL) | ����(��ȡ2g) | ��������״ | �ռ�50 mL��������ʱ��/s |
�� | 10% | �� | ��״ | 70 |
�� | 10% | �� | Ƭ״ | 120 |
�� | 10% | �� | Ƭ״ | 112 |
�� | 20% | �� | Ƭ״ | 110 |
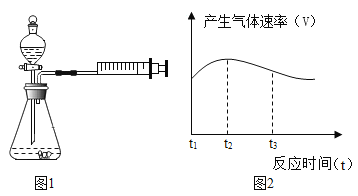
(1)С����С�����ͼ1װ�������Եķ�����:�رշ�Һ©��������������ע�������������ƶ�һ �ξ���,ֹͣ����������,���۲쵽_________________,���ʾ���������á�
(2)д���������ᷴӦ�Ļ�ѧ����ʽ:____________________________________��
���ռ�֤�ݣ�
(3)Ҫ�ȽϽ�������״�Է�Ӧ������Ӱ��,Ӧѡ���ʵ������________________________��
���ó����ۣ�
(4)ͨ�������ĸ�ʵ��,��ó���Ӱ��������ᷴӦ�Ŀ���������________________________��
(5)ʵ������Թ���ڷ���,˵����������ķ�Ӧ�Ƿ��ȷ�Ӧ,ʵ���ø÷�Ӧ�в������������(v)��ʱ��(t)�Ĺ�ϵ��ͼ2��ʾ,����Ϊ��t2~t3ʱ����ڷ�Ӧ������������Ҫԭ����____________________��
��ʵ����չ��
(6)С�������ỻ��ϡ�����������ʵ�飬�������ۺ�ϡ����ķ�Ӧ�������ԡ�Ϊʲô�����������ᷴӦ������ϡ���ᷴӦ��?С����Ϊ������Cl-�Ĵ���ʹ������ķ�Ӧ�����С��������С�����һ��������ʵ������֤����:___________��