题目内容
【题目】实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化,测定结果如图所示。下列说法不正确的是
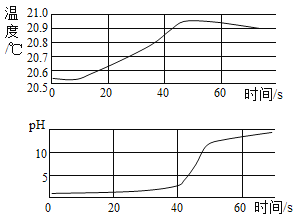
A.反应过程中有热量放出
B.30s时,溶液中溶质为HCI和NaCl
C.从20s到40s,溶液温度升高、pH增大
D.该实验是将稀盐酸滴入稀NaOH溶液中
【答案】D
【解析】
A、由用数字化传感器探究稀氢氧化钠与盐酸反应过程中,温度逐渐升高,说明反应是放热反应,选项正确;
B、由图示可知,30s时溶液的pH小于7,说明稀盐酸过量,所得溶液中的溶质为HCl和NaCl,选项正确;
C、由图示可知,从20 s到40 s,溶液温度升高、pH增大,选项正确;
D、图像中pH值的变化是从小于7逐渐的增大到大于7,可知原溶液显酸性,然后不断的加入碱性溶液,使pH增大,说明是把氢氧化钠溶液滴加到稀盐酸中,选项错误。
故选D。

 名校课堂系列答案
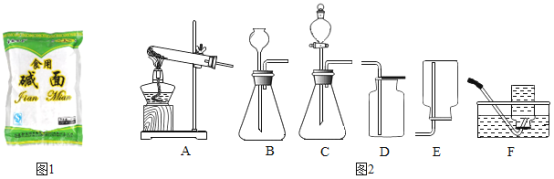
名校课堂系列答案【题目】小明同学在超市里看到“食用碱面”(如图1所示),他想知道该“食用碱面”的成分,请教老师后得知它的主要成分是一种钠盐。
(作出猜想)小明及其他同学猜想其主要成分可能是:
①Na2SO4 ②NaCl ③Na2CO3 ④NaHCO3
(查阅资料)(1)氯化钡溶液与碳酸氢钠溶液不反应。
(2)碳酸氢钠溶液呈碱性。
小明与同学们进行如下实验来确认该“食用碱面”的主要成分。
(进行实验)取适量该“食用碱面”于试管中,加入蒸馏水使之完全溶解,把所得溶液分成两等份。
实验操作 | 实验现象 | 实验结论 |
实验①:在第一份溶液中加入氯化钡溶液 | _____ | 猜想①正确 |
实验②:在第二份溶液中加入_____ | 有气泡产生 | 猜想_____正确 |
(交流讨论)
(1)同学们经过讨论,发现仅仅通过实验①不能得出该“食用碱面”的主要成分是Na2SO4,也可能是Na2CO3,原因是_____(用化学方程式表示)。
(2)同学们通过对实验①②的分析得出该“食用碱面”的主要成分是Na2CO3,理由是_____。
(3)有同学认为把酚酞溶液滴入该“食用碱面”的溶液中,溶液变红,就可得出该“食用碱面”的主要成分是Na2CO3.这种说法对吗?并请说明原因:_____。
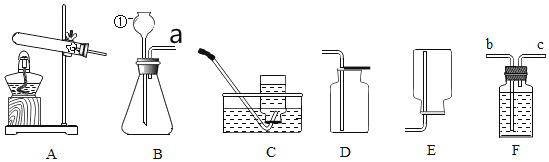
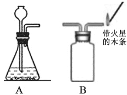
(拓展应用)已知Na2CO3与稀盐酸反应非常剧烈。实验室欲用Na2CO3固体和稀盐酸制取并收集二氧化碳,你选择的装置最好是_____(选填图2中装置序号)。
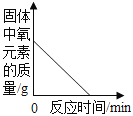
【题目】下列4个图像能正确反映对应变化关系是( )
A | B | C | D |
|
|
|
|
向一定量铁粉中滴加稀盐酸液 | 用酒精灯加热一定量KMnO4固体 | 向一定量澄清石灰水中加入Na2CO3溶液 | 向盛有MnO2的烧杯中加入H2O2溶液 |
A.AB.BC.CD.D