题目内容
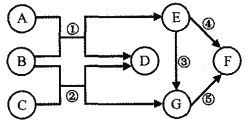
【题目】如图某反应的微观示意图,不同的球代表不同元素的原子,下列说法不正确的是( )

A.该反应为置换反应
B.参加反应的镁原子和二氧化碳分子的微粒个数比是2:1
C.反应涉及的物质中,只有氧化镁属于氧化物
D.在化学变化中,分子可分,原子不可分
【答案】C
【解析】
由微观反应示意图可知,该反应是镁和二氧化碳在点燃的条件下反应生成氧化镁和碳,化学方程式表示为:2Mg+CO2![]() 2MgO+C。
2MgO+C。
A、由化学方程式可知,此反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,属于置换反应,故正确;
B、由化学方程式可知,参加反应的镁原子与二氧化碳分子的个数比为:2:1,故正确;
C、反应涉及到的物质中,二氧化碳和氧化镁都是由两种元素组成的化合物,且其中一种元素是氧元素,所以二者均属于氧化物,故错误;
D、由化学反应的实质可知,在化学变化中,分子可分,原子不可分,故正确。
故选C。

【题目】平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题以此粉末为原料,设计如下工艺流程对资源进行回收,得到Ce(OH)4和硫酸铁铵:
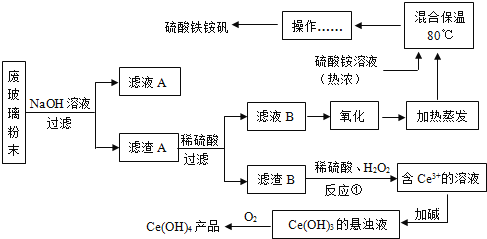
已知:1.SiO2+2NaOH=Na2SiO3+H2O
2.CeO2是一种金属氧化物,化学性质稳定,与稀硫酸不反应。在H2O2存在的条件下,两种物质能反应。
3.硫酸铁铵矾[Fe2(SO4)32(NH4)2SO43H2O]广泛用于水的净化处理.
(1)氧化铈(CeO2)中,铈的化合价为____________,检验硫酸铁铵溶液中含有NH4+的方法是:__________。
(2)为提高①中硫酸的反应效率,可采用的具体措施有_____________。(写一种即可)。
(3)操作应为_____________。
(4)反应①之前先要洗涤滤渣B,其目的是为了除去_____________(填离子符号)。
(5)请补充完整①反应的化学方程式:2CeO2+3H2SO4+H2O2=Ce2(SO4)3+_____+ ____↑。
(6)碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”。实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量的NaCl,加热到一定温度,持续通入SO2,待反应一段时间,过滤得到粗碲。反应方程式为TeOSO4 +2SO2+3H2O![]() Te↓+ 3H2SO4,为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比实验,数据如下:
Te↓+ 3H2SO4,为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比实验,数据如下:
实验 | 温度/℃ | 反应时间 | 粗碲沉淀率/% |
a | 65 | 3.0 | 65.0 |
b | 80 | 3.0 | 98.9 |
c | 80 | 2.0 | 98.9 |
d | 90 | 2.0 | 97.0 |
① a和b的结论是______________。
②为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗确沉淀率。若再设计对比实验,选择的反应条件还可以是_________。
A80℃,1.5h B80℃,2.5h C70℃,
【题目】为了探究影响化学反应速率的因素,某化学兴趣小组的同学设计了如图所示的装置进行实验,收集的相关数据如下表:
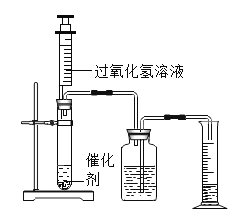
实验序号 | H2O2溶液的浓度% | H2O2溶液的体积/mL | 催化剂/g | 温度/ | 收集相同体积的O2所需的时间/s |
① | 5 | 2 | 0.1gMnO2 | 20 | 18 |
② | 10 | 2 | 0.1gMnO2 | 20 | 6 |
③ | 30 | 8 | 未加 | 40 | 64 |
④ | 30 | 8 | 未加 | 60 | 25 |
⑤ | 10 | a | 0.1gCuO | b | 16 |
(1)过氧化氢溶液与二氧化锰反应的化学方程式____。
(2)由实验_____(填实验序号)知,化学反应速率与H2O2溶液的浓度有关;由实验③和④知,化学反应速率与温度的关系是_____。
(3)表中的数据还反映出不同的催化剂对双氧水溶液分解的催化效果不同,则表中的a=___,b=____