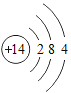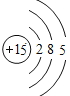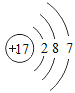题目内容
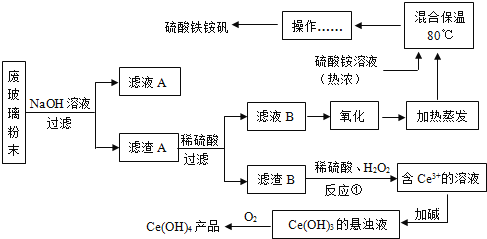
【题目】平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题以此粉末为原料,设计如下工艺流程对资源进行回收,得到Ce(OH)4和硫酸铁铵:
已知:1.SiO2+2NaOH=Na2SiO3+H2O
2.CeO2是一种金属氧化物,化学性质稳定,与稀硫酸不反应。在H2O2存在的条件下,两种物质能反应。
3.硫酸铁铵矾[Fe2(SO4)32(NH4)2SO43H2O]广泛用于水的净化处理.
(1)氧化铈(CeO2)中,铈的化合价为____________,检验硫酸铁铵溶液中含有NH4+的方法是:__________。
(2)为提高①中硫酸的反应效率,可采用的具体措施有_____________。(写一种即可)。
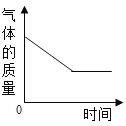
(3)操作应为_____________。
(4)反应①之前先要洗涤滤渣B,其目的是为了除去_____________(填离子符号)。
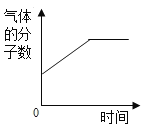
(5)请补充完整①反应的化学方程式:2CeO2+3H2SO4+H2O2=Ce2(SO4)3+_____+ ____↑。
(6)碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”。实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量的NaCl,加热到一定温度,持续通入SO2,待反应一段时间,过滤得到粗碲。反应方程式为TeOSO4 +2SO2+3H2O![]() Te↓+ 3H2SO4,为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比实验,数据如下:
Te↓+ 3H2SO4,为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比实验,数据如下:
实验 | 温度/℃ | 反应时间 | 粗碲沉淀率/% |
a | 65 | 3.0 | 65.0 |
b | 80 | 3.0 | 98.9 |
c | 80 | 2.0 | 98.9 |
d | 90 | 2.0 | 97.0 |
① a和b的结论是______________。
②为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗确沉淀率。若再设计对比实验,选择的反应条件还可以是_________。
A80℃,1.5h B80℃,2.5h C70℃,
【答案】+4 往该溶液中加入烧碱溶液,微热后能产生刺激性气体,并能使湿润的红色石蕊试纸变蓝,证明含有铵根离子 搅拌 降温结晶 Fe3+ 4H2O O2 相同时间内,温度越高,粗碲沉淀率越高 AC
【解析】
(1)氧化铈(CeO2)中,铈的化合价为则有x+(-2)×2=0,x=+4;往该溶液中加入烧碱溶液,微热后能产生刺激性气体,并能使湿润的红色石蕊试纸变蓝,证明含有铵根离子;
(2)为提高①中硫酸的反应效率,可采用搅拌的方法;
(3)据图可知,要从热的浓溶液中得到晶体,应用降温结晶;
(4)洗涤滤渣B的目的是为了除去 Fe3+,提高产品的纯度;
(5)根据现有化学方程式2CeO2+3H2SO4+H2O2═Ce2(SO4)3+ + ,可知反应前:Ce原子有2个,氧原子为18个,硫原子3个,氢原子8个;反应后现有:Ce原子有2个,氧原子为12个,硫原子3个;缺少8个氢原子和6个氧原子,而还有气体生成,所以气体为氧气,所以对应4个水分子和1个氧分子,故填:4H2O和O2;
(6)①由实验a和实验b对比,反应时间一样,反应的温度不一样,所以通过a和b实验得到的结论是:相同时间内,温度越高,粗碲沉淀率越高;
②由表中数据可知,温度为80℃时,不管反应时间是2.0h还是3.0h,粗碲的沉淀率最大都是为98.9%,因此可以对比更短的时间的影响,也可以从节约成本的角度考虑,降低温度,所以选择AC。

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)。
(演示实验)将一定量的稀H2SO4加入盛有NaOH溶液的小烧杯中。
(学生板演)该反应的化学方程式________________。
(提出问题)实验未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
(猜想假设)针对疑问,大家纷纷提出猜想。甲组同学的猜想如下:猜想一:只有Na2SO4;猜想二:有____________ ;猜想三:有Na2SO4和NaOH;猜想四:有Na2SO4、H2SO4和NaOH。乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想及其理由是_________。
(实验探究)
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有____________。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH____7(选填“>”“<”或“=”) | _________ | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有 H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,全班同学一致确定猜想二是正确的。
(评价反思)老师对同学们用多种方法进行探究,并得出正确结论给予肯定。同时指出实验探究(2)中存在两处明显错误,请大家反思。同学们经过反思发现了两处错误:
(1)实验操作中的错误是 __________________ 。
(2)实验方案中有一个是错误的,写出能说明实验方案错误原因的化学方程式是 _______________。
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后瓶中残留废液进行探究。
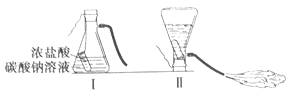
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是______。
(讨论与交流)
小明认为猜想I无需验证就知道是错误的,他的理由是_____(请用化学方程式说明)。
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论____(填“正确”或“错误”),理由是______________。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________________ | __________________ | 猜想3正确 |
(2)验证猜想4,可选择的试剂有____________。
A.酚酞溶液B.氢氧化钾溶液C.稀硫酸D.氯化钡溶液
(拓展与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行____操作,即可从废液中得到NaCl固体。
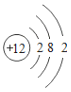
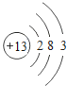
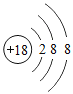
【题目】下表为元素周期表中某一周期元素的原子结构示意图。
元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
原子结构示意图 |
|
|
|
|
|
|
|
|
请回答下列问题:
(1)表中硫原子的核电荷数x=_____,在化学反应中容易_____电子。
(2)表中具有相对稳定结构的元素是_____。
(3)写出铝离子的结构示意图_____。
(4)镁元素与氯元素形成的化合物化学式为_____。
(5)上述元素在周期表中处于同一周期的原因是_____。