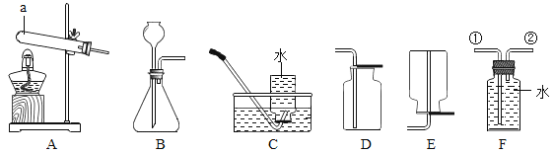
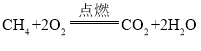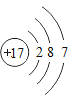题目内容
【题目】下列关于四种粒子的结构示意图的说法中正确的是()
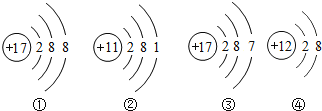
A.①③属于不同种元素
B.②表示的元素在化合物中通常显+1价
C.②③的化学性质相似
D.④属于离子,离子符号为Mg
【答案】B
【解析】
A、同种元素质子数一定相同,①③的质子数都是17,所以两者属于同种元素;故选项错误;
B、由②粒子的结构示意图可知,最外层电子数是1,易失去最外层电子形成带一个单位正电荷的阳离子,故②表示的元素在化合物中通常显+1价,故选项正确;
C、因为元素的性质和最外层电子数关系密切,所以最外层电子数是8(第一层是2)的属稳定结构,由于②③的最外层电子数分别是1、7,所以化学性质不一样,故选项错误;
D、由于离子中质子数与核外电子数不等,而④中质子数比电子数多2是镁离子,其符号应该是Mg2+,故选项错误。
故选:B。

【题目】一些食物的近似pH如下表:
食物 | 苹果 | 葡萄 | 牛奶 | 玉米 |
pH | 2.9~3.3 | 3.5~4.5 | 6.3~6.6 | 6.8~8.0 |
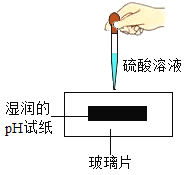
(1)苹果汁和葡萄汁相比较,酸性较强的是________,它能使石蕊试液变________色。
(2)人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜食用的食物是________。
(3)鸡蛋壳中含有CaCO3,以前因胃酸过多导致胃痛时,有人吃鸡蛋壳粉。现今,许多冶疗胃酸过多的药品的有效成分是氢氧化铝,而不是CaCO3,提出一种理由说明为什么氢氧化铝优越于碳酸钙________,写出氢氧化铝与胃酸反应的化学方程式________。
【题目】小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用的办法如下:取用8 g这种石灰石样品,把40 g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。请计算:
(1)8 g石灰石样品中含有杂质多少克____________?
(2)样品中碳酸钙的质量分数是多少_________________?
(3)下表中m的数值应该为多少____________?
序号 | 加入稀盐酸质量/g | 剩余固体质量/g |
第1次 | 10 | 5.5 |
第2次 | 10 | m |
第3次 | 10 | 1.2 |
第4次 | 10 | 1.2 |
(4)要得到280 kg CaO,需要质量分数为80%的石灰石多少千克_____________?(化学方程式:CaCO3![]() CaO+CO2↑)
CaO+CO2↑)