题目内容
【题目】我们生活在空气中,没有空气我们将无法生存,请你参与到化学兴趣小组关于气体的制取与性质的研究中,贡献你的聪明和才智。

探究一
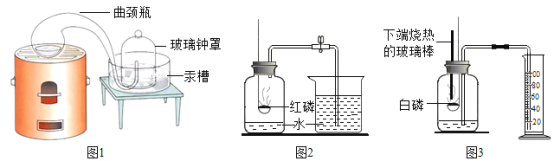
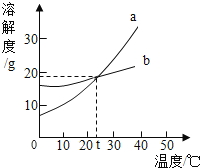
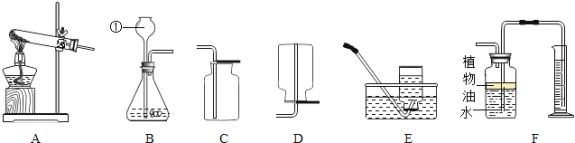
如图1是实验室制取气体的部分装置,请回答下列问题:
氢气是最理想的燃料。通常状况下,氢气密度比空气小,难溶于水。小秦同学用锌粒与盐酸反应制取氢气,选择的装置组合是______(填字母),该发生装置的优点是____________________________,若用F装置排空气法收集氢气,气体应从___端进入(填b或c)。
探究二
(提出问题)①导出的气体除H2外,还有哪些气体?
②氢气具有可燃性外,还具有什么化学性质?
(查阅资料)无水CuSO4是白色的粉末,遇水变为蓝色;碱石灰是氢氧化钠和氧化钙的固体混合物。
(设计实验方案)小泰同学按如图2装置进行实验(假设每个装置中气体都完全反应或吸收)。
(实验现象和结论)
实验现象 | 实验结论 |
甲装置中的白色固体变成蓝色 | 气体中有H2O |
乙装置中产生______________ | 气体中有HCl |
丁装置中玻璃管内红色粉末变成黑色、戊装置中白色固体变成蓝色 | H2能与Fe2O3反应丁装置中玻璃管内反应的化学方程式为 ______ (写加热也可) |
(交流总结)
丁装置加热前通入H2的目的是____________________。
【答案】BC或BD,可以随时控制反应的发生或停止,c;白色沉淀,:3H2+Fe2O3![]() 2Fe+3H2O;排净装置内的空气,防止加热时发生爆炸
2Fe+3H2O;排净装置内的空气,防止加热时发生爆炸
【解析】
探究一、锌粒与盐酸反应制取氢气,属于固液常温下反应制取气体,选择的发生装置是B,由于氢气密度比空气小,难溶于水,选择的收集装置是C或D,该发生装置的优点是通过关闭或打开活塞,可以随时控制反应的发生或停止,若用F装置排空气法收集氢气,由于氢气密度比空气小,气体应从c端进入;
探究二、实验现象和结论:由于氯化氢气体溶于水生成盐酸,盐酸能与硝酸银反应生成了氯化银白色沉淀,所以乙装置中的现象是产生了白色沉淀,在加热的条件下氢气与氧化铁的反应生成了铁和水,反应的化学方程式是:3H2+Fe2O3![]() 2Fe+3H2O;
2Fe+3H2O;