题目内容
【题目】学习氧气的制取和性质时,某化学兴趣小组用下列装置进行有关探究:
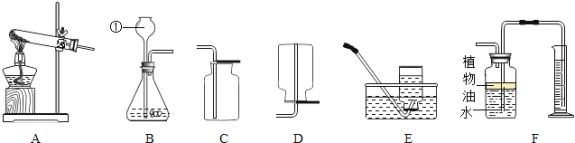
(1)他们用加热高锰酸钾的方法制取氧气,其主要操作有:①装药品;②检查装置的气密性;③固定装置;④加热;⑤收集气体;⑥撤酒精灯;⑦从水槽中撤出导气管.
正确的操作顺序是______.有关反应的文字表达式是______.
(2)当导管口开始有气泡产生时,不宜立即收集,原因是______;
(3)检验制得的气体是否是氧气的方法是______.他们用制得的氧气做铁丝燃烧的实验,结果发现集气瓶炸裂了,其原因是______.F装置可用来测定制得氧气的体积,对进入量筒里的水读数时,我们的视线应______.
(4)小组成员小慧同学想用氯酸钾制取一瓶氧气,误把高锰酸钾当成二氧化锰,加热时氯酸钾的反应速率也很快.于是她惊奇地告诉同学舒展:高锰酸钾也可以作为氯酸钾分解的催化剂.小明经过思考后,认为小慧的结论不科学. 你认为高锰酸钾能加快氯酸钾分解的原因是___.高锰酸钾是否是该反应的催化剂呢?______(填“是”或“否”).
【答案】②①③④⑤⑦⑥高锰酸钾![]() 锰酸钾+二氧化锰+氧气装置中有空气,会造成收集的氧气不纯将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气试管底部没有放入水或细沙与量筒内凹液面的最低处保持平衡高锰酸钾受热分解时生成了二氧化锰否
锰酸钾+二氧化锰+氧气装置中有空气,会造成收集的氧气不纯将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气试管底部没有放入水或细沙与量筒内凹液面的最低处保持平衡高锰酸钾受热分解时生成了二氧化锰否
【解析】
(1)实验室制取氧气的主要操作步骤是:检验装置的气密性;加入药品;加热;收集气体;从水槽中取出导管;停止加热。故正确的操作顺序为②①③④⑤⑦⑥;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的文字表达式为高锰酸钾![]() 锰酸钾+二氧化锰+氧气;
锰酸钾+二氧化锰+氧气;
(2)当导管口开始有气泡产生时,不宜立即收集,原因是气体发生装置中有空气,会造成收集的氧气不纯;
(3)氧气的检验方法是将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气;用制得的氧气做铁丝燃烧的实验,集气瓶的底部要放少量水或细沙,否则集气瓶会因溅落黑色熔融物引起炸裂;对进入量筒里的水读数时,我们的视线应与量筒内凹液面的最低处保持水平;
(4)高锰酸钾能加快氯酸钾分解的原因是:高锰酸钾受热分解时生成了二氧化锰,因此高锰酸钾不是该反应的催化剂,起催化作用的是二氧化锰;

【题目】我们生活在空气中,没有空气我们将无法生存,请你参与到化学兴趣小组关于气体的制取与性质的研究中,贡献你的聪明和才智。

探究一
如图1是实验室制取气体的部分装置,请回答下列问题:
氢气是最理想的燃料。通常状况下,氢气密度比空气小,难溶于水。小秦同学用锌粒与盐酸反应制取氢气,选择的装置组合是______(填字母),该发生装置的优点是____________________________,若用F装置排空气法收集氢气,气体应从___端进入(填b或c)。
探究二
(提出问题)①导出的气体除H2外,还有哪些气体?
②氢气具有可燃性外,还具有什么化学性质?
(查阅资料)无水CuSO4是白色的粉末,遇水变为蓝色;碱石灰是氢氧化钠和氧化钙的固体混合物。
(设计实验方案)小泰同学按如图2装置进行实验(假设每个装置中气体都完全反应或吸收)。
(实验现象和结论)
实验现象 | 实验结论 |
甲装置中的白色固体变成蓝色 | 气体中有H2O |
乙装置中产生______________ | 气体中有HCl |
丁装置中玻璃管内红色粉末变成黑色、戊装置中白色固体变成蓝色 | H2能与Fe2O3反应丁装置中玻璃管内反应的化学方程式为 ______ (写加热也可) |
(交流总结)
丁装置加热前通入H2的目的是____________________。
【题目】如下表:原子结构是通过科学家不断地建立与修正原子结构模型,不断地实验,不断地思考研究而得到的.下表是原子结构模型的几种学说
时间 | 模型类型 | 科学家 | 内容 |
| 道尔顿模型 | 道尔顿(英国) | 原子是一个坚硬的小球 |
| 汤姆生模型 | 汤姆生(英国) | 发现电子,即“西瓜模型”正电荷是西瓜肉,电子是西瓜籽 |
| 卢瑟福模型 | 卢瑟福(英国) | 发现原子核,原子大部分体积是空的,电子围绕带正电的原子核随意动转 |
| 分层模型 | 玻尔(丹麦) | 电子在固定轨道上分层运动(绕着原子核) |
现代 | 电子云模型 | 电子出现在原子核周围,有的区域次数多,有的区域次数少 |
![]() 上面四种原子结构模型中道尔顿的原子结构模式是________(填序号),这种原子模型是一种________结构.
上面四种原子结构模型中道尔顿的原子结构模式是________(填序号),这种原子模型是一种________结构.
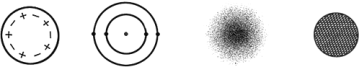
![]() 年,______通过实验发现原子结构,所做的实验名称是________,实验中大多数
年,______通过实验发现原子结构,所做的实验名称是________,实验中大多数![]() 微粒不改变原来的运动方向,顺利通过.有一小部分
微粒不改变原来的运动方向,顺利通过.有一小部分![]() 微粒发生了偏转,原因是________;极少数
微粒发生了偏转,原因是________;极少数![]() 微粒被反弹了回来,原因是________.因此,卢瑟福根据实验建立了________原子模型.
微粒被反弹了回来,原因是________.因此,卢瑟福根据实验建立了________原子模型.
![]() 请用框图的形式表示原子的结构:
请用框图的形式表示原子的结构:
【题目】下图是铁丝在氧气中燃烧实验的操作图。试回答下列问题:
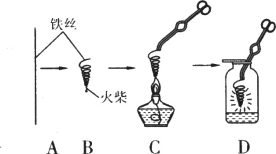
(1)B图中螺旋形铁丝的一端系一根火柴的作用是_________________。
(2)D图中集气瓶底装入少量的水,目的是_______________________。
(3)写出铁丝在氧气中燃烧的文字表达式______________________________。
(4)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录。
请你分析回答:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填写 |
你认为表中未填的实验现象是________________________________。造成铁丝在氧气中燃烧时火星四射的主要原因是________________________________。