题目内容
【题目】金属材料与人类的生产和生活密切相关。回答:
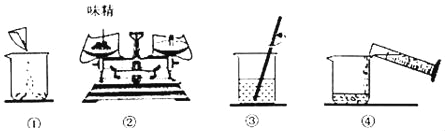
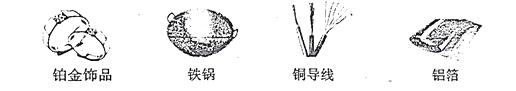
(1)根据下列金属制品在生活中的用途,推断金属具有的物理性质有__________(写出一条即可)。
(2)金属活动性顺序是化学重要规律之一,下列关于实验的说法正确的是__________(填序号)。
A.铝丝伸进硫酸铜溶液前需要用砂纸打磨
B.铜与稀硫酸反应,有细小气泡生成
C.银能将硝酸铜溶液中的铜置换出来
D.铁、镁、铜、金四种金属分别放在灯焰上灼烧,铜和金没变化
(3)自行车车架表面喷漆不仅美观,而且可有效防止铁与空气中的__________接触而生锈。
(4)钛酸亚铁(FeTiO3)在一定条件下发生反应为2FeTiO3+6C+7Cl2 ![]() 2FeCl3+2TiCl4+6X,则X的化学式为__________。
2FeCl3+2TiCl4+6X,则X的化学式为__________。
(5)向Al(NO3)3、AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤渣中滴加稀盐酸时看气泡产生。则滤渣中含有__________(写名称),滤液中含有的金属离子有__________(写符号)。
(6)用一氧化碳冶炼2000t含杂质3%的生铁,需要含四氧化三铁90%的磁铁矿的质量是___________t(结果精确到0.1)。
【答案】光泽 导热性 导电性 延展性(任写一条)A氧气和水CO银和锌Al3+和Zn2+2976.7
【解析】
根据已有的金属的物理性质和化学性质及用途、质量守恒定律的知识以及根据化学方程式的计算的知识进行分析解答即可。
(1)铂金饰品利用的是金属的光泽,铁锅利用的是金属的导热性,铜导线利用的是金属的导电性,铝箔利用的是金属的延展性;
(2)A、铝易被氧气氧化生成致密的氧化铝保护膜,故铝丝伸进硫酸铜溶液前需要用砂纸打磨,正确;B、铜在氢的后面,不能与稀硫酸反应,错误;C、银的活动性比铜弱,故银不能将硝酸铜溶液中的铜置换出来,错误;D、铁、镁、铜、金四种金属分别放在灯焰上灼烧,金没变化,铜会变黑,错误。故填A;
(3)根据钢铁锈蚀的条件,自行车车架表面喷漆能有效防止铁与空气中的水和氧气接触而生锈;
(4)根据2FeTiO3+6C+7Cl2 ![]() 2FeCl3+2TiCl4+6X,反应前含有2个Fe原子,2个Ti原子,6个O原子,6个C原子,14个Cl原子,反应后含有2个Fe原子,2个Ti原子,14个Cl原子,则6X中含有6个O原子,6个C原子,故X是一氧化碳,化学式为CO;
2FeCl3+2TiCl4+6X,反应前含有2个Fe原子,2个Ti原子,6个O原子,6个C原子,14个Cl原子,反应后含有2个Fe原子,2个Ti原子,14个Cl原子,则6X中含有6个O原子,6个C原子,故X是一氧化碳,化学式为CO;
(5)向Al(NO3)3、AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤渣中滴加稀盐酸时有气泡产生,说明金属有锌,锌过量,则银全部被置换出来,则滤渣中含有 锌和银,滤液中含有的金属离子有 Al3+、Zn2+;
(6)解:设用一氧化碳冶炼2000t含杂质3%的生铁,需要含四氧化三铁90%的磁铁矿的质量为x
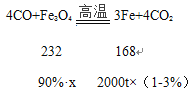
![]()
x≈2976.7t。
答:需要含四氧化三铁90%的磁铁矿的质量是2976.7t。

【题目】小君和小英同学发现:带火星的竹签在空气中不会复燃,若用装有60%水的集气瓶倒置在水槽中收集氧气,得到的气体能使带火星的竹签复燃,为了找到能使带火星竹签复燃的氧气含量最小值,他们进行了如下探究:
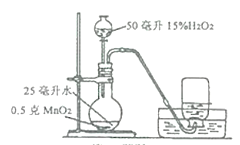
(1)(设计实验)小君设计了如图的装置,该装置的圆底烧瓶中放入25毫升水的目的是___。
(实验研究)第一组实验:取3只集气瓶,编号为①②③,分别装入15%、30%和45%的水,盖上盖玻片倒置在水槽中。当气泡___放出后,导管口伸入集气瓶把其中的水全部排出,将相同的3支带火星竹签分别插入①~③号瓶中,记录实验现象。
获得第一组实验现象后,小君又做了第二组实验,并记录实验现象,两组实验数据和现象见下表:
实验分组 | 第一组 | 第二组 | ||||
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
集气瓶装水的体积分数/% | 15 | 30 | 45 | 34 | 38 | 42 |
带火星竹签状况 | 亮 | 很亮 | 复燃 | 很亮 | 复燃 | 复燃 |
(2)使用带火星的木条验满氧气的方法是否可靠:_____(填“是”或“否’')。
(3)集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数×___%.
(4)根据两组实验现象得出,收集的氧气占容积的体积分数最低为____%时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数分数是__%(计算结果保留整数)。
(5)小英认为上述两组实验现象还不能确定能使带火星竹签复燃的氧气含量最小值,需继续进行实验。则实验序号⑦的集气瓶装水的体积分数应该是____%。
(6)(实验结论)再经过数次实验并计算后得出:能使带火星竹签复燃的氧气含量最小值为48.7%。
(继续探究)小君认为采用该方法收集的氧气中含有一定量的水蒸气,请你提出实验改进的措施___。
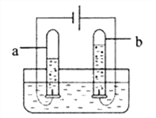
(7)为了测定能使带火星的木条复燃时氧气的最低浓度,课外活动小组的同学们又进行了实验探究。他们设计的实验方案是先将氧气和空气按不同的体积比收集在集气瓶里。收集气体的装置如图。
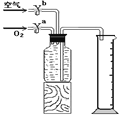
收集气体的方法是:在150mL集气瓶里装满水,塞紧胶塞并关闭活塞 b,打开活塞a通入氧气,把瓶里的水排入量筒,当量筒内的水达到设定的体积后立即关闭活塞a,然后打开活塞b通入空气,把瓶里的水全部排入量筒。若要收集一瓶含氧气的体积分数约为60%的气体,则停止通入氧气时量筒内水的体积约为_____(提示:空气中氧气的体积分数约为1/5)
A.25 mLB.40 mL C.60 mL D.75 mL
【题目】甲、乙、丙三种物质间通过一步反应能实现右图转化,下列选项中符合图示转化关系的是
选项 | 甲 | 乙 | 丙 |
A | NaOH | NaCl | NaNO3 |
B | CuO | CuCl2 | Cu(OH)2 |
C | Na2CO3 | CO2 | CaCO3 |
D | H2O2 | H2O | O2 |

A. A B. B C. C D. D
【题目】我们生活在空气中,没有空气我们将无法生存,请你参与到化学兴趣小组关于气体的制取与性质的研究中,贡献你的聪明和才智。

探究一
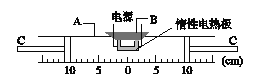
如图1是实验室制取气体的部分装置,请回答下列问题:
氢气是最理想的燃料。通常状况下,氢气密度比空气小,难溶于水。小秦同学用锌粒与盐酸反应制取氢气,选择的装置组合是______(填字母),该发生装置的优点是____________________________,若用F装置排空气法收集氢气,气体应从___端进入(填b或c)。
探究二
(提出问题)①导出的气体除H2外,还有哪些气体?
②氢气具有可燃性外,还具有什么化学性质?
(查阅资料)无水CuSO4是白色的粉末,遇水变为蓝色;碱石灰是氢氧化钠和氧化钙的固体混合物。
(设计实验方案)小泰同学按如图2装置进行实验(假设每个装置中气体都完全反应或吸收)。
(实验现象和结论)
实验现象 | 实验结论 |
甲装置中的白色固体变成蓝色 | 气体中有H2O |
乙装置中产生______________ | 气体中有HCl |
丁装置中玻璃管内红色粉末变成黑色、戊装置中白色固体变成蓝色 | H2能与Fe2O3反应丁装置中玻璃管内反应的化学方程式为 ______ (写加热也可) |
(交流总结)
丁装置加热前通入H2的目的是____________________。