题目内容
【题目】一定质量的CH4可与常见物质M反应,同时放出少量热量;将所得产物Cu2O与O2反应又生成M,同时放出较多热量。其反应原理如下图所示。下列说法正确的是

A.M中铜元素的质量分数比Cu2O中的高
B.理论上反应每生成44gCO2,同时生成18gH2O
C.理论上每16gCH4参与反应,最终消耗64gO2
D.过程①可将CH4中的部分能量储存于Cu2O中
【答案】C
【解析】
如图所示,CH4与常见物质M反应生成Cu2O、二氧化碳和水,Cu2O与O2反应生成M,则M为CuO,则有:
A、CuO中铜元素的质量分数为![]() ,Cu2O中铜元素的质量分数为
,Cu2O中铜元素的质量分数为![]() ,Cu2O中铜元素的质量分数比CuO中的高,A选项说法不正确,不符合题意;
,Cu2O中铜元素的质量分数比CuO中的高,A选项说法不正确,不符合题意;
B、根据反应过程、由元素守恒可知生成物二氧化碳中的碳元素来自于甲烷,水中的氢元素来自于甲烷,44gCO2中碳元素的质量为![]() ,则参加反应的甲烷的质量为
,则参加反应的甲烷的质量为![]() ,设16g甲烷反应生成水的质量为
,设16g甲烷反应生成水的质量为![]() ,由氢元素守恒则有
,由氢元素守恒则有![]() ,解得
,解得![]() ,因此理论上反应每生成44gCO2,同时生成36gH2O,B选项说法不正确,不符合题意;
,因此理论上反应每生成44gCO2,同时生成36gH2O,B选项说法不正确,不符合题意;
C、由反应过程可知,CH4与常见物质CuO反应生成Cu2O、二氧化碳和水,反应的方程式为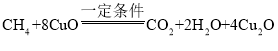 ,由方程式可知每16份质量的甲烷与640份质量的氧化铜恰好反应,Cu2O与O2反应生成CuO,反应的方程式为
,由方程式可知每16份质量的甲烷与640份质量的氧化铜恰好反应,Cu2O与O2反应生成CuO,反应的方程式为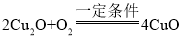 ,由方程式可知每32份质量的氧气参与反应生成320份质量的氧化铜,由两个反应之间的关系可知理论上每16份质量的CH4参与反应,最终消耗64份质量的O2,即理论上每16gCH4参与反应,最终消耗64gO2,C选项说法正确,符合题意;
,由方程式可知每32份质量的氧气参与反应生成320份质量的氧化铜,由两个反应之间的关系可知理论上每16份质量的CH4参与反应,最终消耗64份质量的O2,即理论上每16gCH4参与反应,最终消耗64gO2,C选项说法正确,符合题意;
D、过程①CH4与常见物质M反应生成Cu2O、二氧化碳和水,该过程释放能量,可将反应物CH4和M中的部分能量储存于Cu2O、二氧化碳和水中,D选项说法不正确,不符合题意。故选C。

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案【题目】超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中Na2CO3的质量分数。他们取了6g纯碱样品放入烧杯中,再将80g一定溶质质量分数的稀盐酸分4次加入该烧杯中,充分反应后测得实验数据如下表(不考虑CO2溶解于水)
实验次数 | 1 | 2 | 3 | 4 |
加人稀盐酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物质的质量/g | 25.2 | m | 63.8 | 83.8 |
(1)表格中m的值为_____。
(2)样品中Na2CO3的质量分数是多少? (写出计算过程,计算结果精确到0.1%)