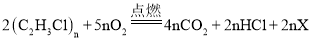题目内容
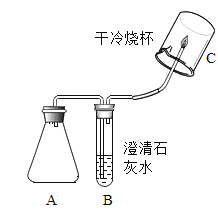
【题目】化学兴趣小组的同学在探究碱的化学性质时,完成了如图1所示的实验。

请你完成下列问题:
(1)第一组同学在向A中加入一定量的稀盐酸后,发现A中溶液仍然呈红色,则反应后溶液中的溶质是_____(酚酞除外,用化学式表示)。
(2)第二组同学做完A实验后溶液呈无色,用微观理论解释A中溶液变为无色的反应的实质是_____。
(3)第三组同学做B实验用于确认二氧化碳与氢氧化钠能发生化学反应(实验前K1、K2均处于关闭状态)。B实验全过程的操作及现象如表:
步骤 | 现象 |
第一步:打开_____,液体流下后,快速使其恢复关闭状态。 | 气球膨胀 |
第二步:_____ | 气球又收缩至原来状态 |
请写出导致气球膨胀的化学反应方程式_____。
(4)实验结束后,小军将以上同学做的A、B两个实验的废液均倒入同一个大烧杯中,观察到混合后的废液呈红色,由此产生疑问:
[提出问题]大烧杯的废液中含有哪些溶质?(酚酞除外)
[查阅资料]氯化钙溶液呈中性,![]()
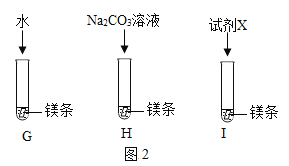
[实验验证]取一定量的废液,逐滴加入氯化钙溶液,如图2为同学们根据部分实验现象绘制的关系曲线。
[实验结论]如果观察到的现象只有沉淀产生,溶液仍然为红色,则废液中的溶质为(填化学式)_____;如果观察到有沉淀产生,溶液由红色变为无色,则废液中的溶质为(填化学式)_____。
【答案】NaCl和NaOH 氢氧根离子和氢离子结合成水 K1 打开K2,液体流下后,快速使其恢复关闭状态 ![]() NaOH、NaCl、Na2CO3、 NaCl、Na2CO3
NaOH、NaCl、Na2CO3、 NaCl、Na2CO3
【解析】
(1) 第一组同学在向A中加入一定量的稀盐酸后,发现A中溶液仍然呈红色,说明溶液呈碱性,溶液中的溶质有:NaCl 和NaOH。
(2)第二组同学做完A实验后溶液呈无色,用微观理论解释A中溶液变为无色的反应的实质是:氢氧根离子和氢离子结合成水。
(3)第一步:B实验中,打开K1时,氢氧化钠和二氧化碳反应,生成碳酸钠和水,使瓶内压强减小,在大气压的作用下,气球鼓起。
第二步:打开K2,液体流下后,快速使其恢复关闭状态,盐酸与反应生成的碳酸钠反应生成二氧化碳,使瓶内的压强增大,小气球重新变瘪。
导致气球膨胀的化学反应为氢氧化钠和二氧化碳反应,生成碳酸钠和水,化学方程式为:![]() 。
。
(4)[实验结论]
反应过程中有氯化钠生成,大烧杯的废液中一定存在氯化钠。碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠。如果观察到的现象只有沉淀产生,溶液仍然为红色,说明碳酸钠反应完后溶液还呈碱性,溶液中含有氢氧化钠,则废液中的溶质为NaCl、Na2CO3、 NaOH;如果观察到有沉淀产生,溶液由红色变为无色,则废液中没有氢氧化钠,废液中的溶质是:![]() 、Na2CO3。
、Na2CO3。

【题目】2020年一场抗击新冠肺炎的战疫在全球展开,一些消毒剂再次走进了百姓家。下表是几种消毒剂,请完成下列问题:
序号 | ① | ② | ③ | ④ |
消毒剂 | 医用酒精 | 二氧化氯 | 过氧乙酸 | “84”消毒液 |
主要成分 | C2H5OH | ClO2 | CH3COOOH | NaClO |
(1)其主要成分属于有机物的是_____(填序号,下同),属于氧化物的是_____。
(2)制备“84”消毒液主要成分次氯酸钠(NaCIO)的化学方程式为![]() ,则X的化学式为_____;次氯酸钠中氯元素的化合价是_____价。
,则X的化学式为_____;次氯酸钠中氯元素的化合价是_____价。
(3)过氧乙酸是一种无色透明的液体,有刺激性气味,易溶、挥发,易分解,有强酸性。
①用100g质量分数为10%的过氧乙酸溶液配制2%的该溶液,需水_____mL。
②下列关于过氧乙酸,说法正确的是_____(填序号)。
A 该物质可用于铁质容器的消毒
B 配制溶液时应帶橡胶手套,防止药液溅到皮肤上
C 如果药品不慎溅入眼中或皮肤上,应立即用氢氧化钠溶液冲洗
D 该物质适合长期放置使用