题目内容
【题目】实验是学习化学的一条重要途径。请回答问题:

(1)如图一,观察到蜡烛燃烧时火焰分为a、b、c三层,其中温度最高的是____(填字母序号)。
(2)如图二,取一个冷而干燥的小烧杯罩在火焰上方,观察到烧杯内壁出现_____,快速倒转烧杯,倒入少量澄清石灰水,振荡,观察到澄清石灰水变浑浊。由此可知,蜡烛燃烧后的产物一定有H2O和______(填化学式)。
(3)如果用一个大烧杯扣住蜡烛(如图三),一段时间后,观察到蜡烛熄灭,说明燃烧需要____。
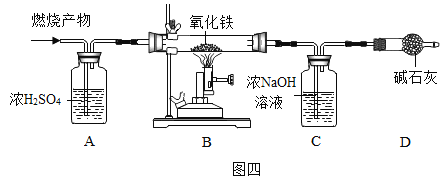
(4)为测定某有机物的组成(如图四),往装置中先通入一段时间干燥的氮气,再将6.4g样品在氧气中燃烧后的产物(样品无剩余)依次通过装置A、B、C、D(装置中涉及的每步反应均反应完全),结果发现装置A增重7.2g,装置C增重8.8g。试
①装置A中利用了浓硫酸的________。
②装置B中红色粉末变成黑色的原因是_____(用化学方程式表示)。
③装置C中反应的化学方程式为_________。
④由此可知,该有机物化学式中碳、氧原子的个数比为________(填最简整数比)。
【答案】a 水雾 CO2 氧气 吸水性 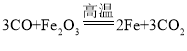 2NaOH+CO2=Na2CO3+H2O 1:1
2NaOH+CO2=Na2CO3+H2O 1:1
【解析】
根据蜡烛火焰分为外焰、内焰、焰心三层,石蜡燃烧后生成水和二氧化碳;燃烧的条件;一氧化碳和氧化铁的反应、氢氧化钠和二氧化碳反应,以及化学反应前后原子的种类、数目和质量不变进行分析作答。
(1)蜡烛火焰分为a、b、c三层,对应为外焰、内焰、焰心,外焰燃烧最充分,蜡烛火焰的外焰温度最高;
(2)蜡烛的主要成分是石蜡,石蜡燃烧后生成水和二氧化碳;用干冷的烧杯罩在火焰上方,会观察到在烧杯内壁有水雾产生,说明蜡烛燃烧生成了水;快速倒转烧杯,倒入少量澄清石灰水,振荡,观察到澄清的石灰水变浑浊,说明蜡烛燃烧还生成二氧化碳;
(3)如图三,用一个大烧杯罩住一支点燃的蜡烛,一段时间后熄灭是因为耗尽了氧气,这说明可燃物燃烧需要氧气;
(4)①装置A中利用了浓硫酸的吸水性;
②装置B中红色粉末变成黑色的反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,反应条件是高温,化学方程式表示为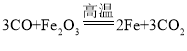 ;
;
③装置C中的反应是氢氧化钠溶液和二氧化碳反应,生成物是碳酸钠和水,化学方程式为2NaOH+CO2=Na2CO3+H2O;
④装置A增重7.2g,浓硫酸吸收水,即反应生成水的质量7.2g,其中氢元素质量:![]() ;
;
装置C增重8.8g,是因为氢氧化钠溶液和二氧化碳反应,即反应生成二氧化碳质量8.8g,其中碳元素质量:![]() ;
;
该有机物中氧元素的质量是6.4g-2.4g-0.8g=3.2g,则该有机物化学式中碳、氧质量比是:2.4g:3.2g =3:4,则该有机物化学式中碳、氧原子的个数比为![]() =1:1。
=1:1。

【题目】化学兴趣小组的同学在探究碱的化学性质时,完成了如图1所示的实验。

请你完成下列问题:
(1)第一组同学在向A中加入一定量的稀盐酸后,发现A中溶液仍然呈红色,则反应后溶液中的溶质是_____(酚酞除外,用化学式表示)。
(2)第二组同学做完A实验后溶液呈无色,用微观理论解释A中溶液变为无色的反应的实质是_____。
(3)第三组同学做B实验用于确认二氧化碳与氢氧化钠能发生化学反应(实验前K1、K2均处于关闭状态)。B实验全过程的操作及现象如表:
步骤 | 现象 |
第一步:打开_____,液体流下后,快速使其恢复关闭状态。 | 气球膨胀 |
第二步:_____ | 气球又收缩至原来状态 |
请写出导致气球膨胀的化学反应方程式_____。
(4)实验结束后,小军将以上同学做的A、B两个实验的废液均倒入同一个大烧杯中,观察到混合后的废液呈红色,由此产生疑问:
[提出问题]大烧杯的废液中含有哪些溶质?(酚酞除外)
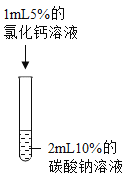
[查阅资料]氯化钙溶液呈中性,![]()
[实验验证]取一定量的废液,逐滴加入氯化钙溶液,如图2为同学们根据部分实验现象绘制的关系曲线。
[实验结论]如果观察到的现象只有沉淀产生,溶液仍然为红色,则废液中的溶质为(填化学式)_____;如果观察到有沉淀产生,溶液由红色变为无色,则废液中的溶质为(填化学式)_____。
【题目】空气质量意味着生活质量。
(1)下表为某同学测量的呼吸前后气体组成的实验数据(通常状况).
物质 | 吸入空气(体积分数/%) | 呼出气体(体积分数/%) |
氮气 | 78 | 75 |
氧气 | 21 | 16 |
二氧化碳 | 0.03 | 4 |
水蒸气 | a | b |
①氮气的化学性质比较_________(填“稳定”或“活泼”),在呼吸前后没有发生变化,实验中呼出气体的总体积_________吸入空气的总体积(填“>”“=”或“<”)。
②呼吸时消耗O2产生CO2,该过程______能量(填“吸收”或“释放”)。呼吸前后气体中水蒸气含量变化较大,实验中其体积分数b_________a(填“>”“=”或“<”)。
(2)汽车多以汽油为燃料,辛烷(C8H18)是汽油中的一种成分。
①每114gC8H18完全燃烧,需要消耗400gO2,生成mgCO2和162gH2O,则m=_______g。
②与完全燃烧相比,等质量的C8H18不完全燃烧时会产生CO,消耗O2的质量_______(填“偏大”“相等”或“偏小”),除污染环境外,燃料不完全燃烧还会产生的问题是_______(写出一种)。
(3)“远在高空是地球卫士,近在身边是健康杀手。”臭氧(O3)对环境的作用需辩证地认识。
①高空中臭氧层能吸收紫外线,有学者认为,致冷剂氟利昂进入高空大气后会产生氯原子(C1),引发以下反应:![]() Ⅰ
Ⅰ
![]() Ⅱ
Ⅱ
Cl加快了上述转化过程总反应的速率,但自身的质量和化学性质在总反应前后没有发生变化,其作用是_________,该转化过程总反应的化学方程式为__________。
②地面附近的臭氧是一种空气污染物,臭氧属于________(填“单质”或“化合物”),O3可表示一个___________(填“原子”“分子”或“离子”)。
(4)有人提出:你吸入的空气中的某个氧原子可能自于若干年前恐龙的身体。该说法表达的观点是_____(填字母)。
A 分子聚集形成物质,分子在不停地运动
B 在化学变化中原子既不会产生,也不会消失
C 原子内部结构复杂,原子不是构成物质的最小微粒
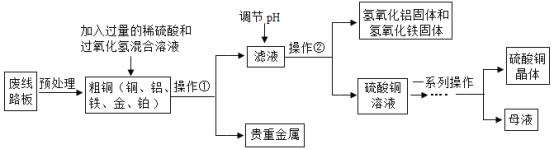
【题目】化学课堂上,同学们分小组合作探究碳酸钠的性质,请你参与探究并填空。
(实验记录与分析)
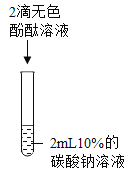
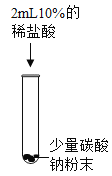
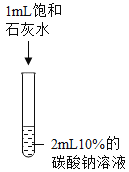
实验一 | 实验二 | 实验三 | 实验四 | |
实验操作 |
|
|
|
|
实验现象 | 溶液由无色变为红色 | _______ | 生成白色沉淀 | 生成白色沉淀 |
实验结论 | 碳酸钠溶液显____性 | 碳酸钠能与盐酸发生反应 | 碳酸钠能与氢氧化钙发生反应 | ______ |
(反思与拓展)
(1)甲同学分析实验一得出:盐溶液____(选填“一定”或“不一定”)显中性。
(2)乙同学用稀硫酸代替实验二中的稀盐酸进行探究,发现实验现象相同。从微观角度分析,这是因为稀盐酸和稀硫酸中都含有_____。
(3)丙同学对比实验三和实验四的现象,从微观角度分析,两个反应的实质相同,溶液中相互结合的离子都是_______。