题目内容
【题目】我国塑料购物袋的年消耗量很大,废弃塑料的处理亟待解决。回答下列问题。
(1)购物袋等塑料制品的大量使用,可能会造成的一种环境污染是____________。
(2)小林尝试用焚烧法对某类塑料购物袋(主要成分是聚氯乙烯)进行处理,并将燃烧产物用氢氧化钠溶液进行吸收。
(查阅资料)I.聚氯乙烯的化学式为(C2H3C1)n
Ⅱ.氯化氢气体会污染环境
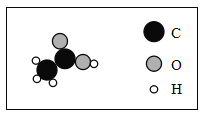
Ш.![]()
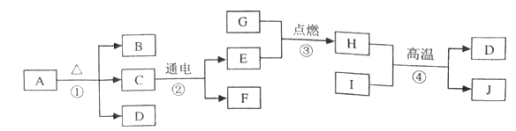
①聚氯乙烯完全燃烧的化学方程式如下: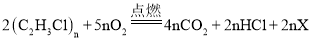 ,则X的化学式为____________。
,则X的化学式为____________。
②将完全燃烧后的产物,全部通入到一定量的NaOH溶液中,得到吸收液,写出氢氧化钠溶液吸收氯化氢的化学方程式___________________。
③小林对吸收液的溶质成分产生了兴趣,进行如下探究:
(提出问题)吸收液中溶质的成分是什么?
(进行实验1)取吸收液少许置于试管中,滴加2~3滴无色酚酞试液,发现酚酞变红色,说明溶液呈_____性。
(猜想)猜想1:NaCl、NaOH、Na2CO3
猜想2:____________。
猜想3:NaCl、Na2CO3、NaHCO3
猜想4:NaCl、NaHCO3
(进行实验2)向实验1所得溶液中,加入过量的CaCl2溶液,小林观察到____________。(填实验现象),最终得出结论:猜想1正确。
(交流反思)实验结束后,小林对吸收液进行无害化处理,其方案是____________,然后倒入废液缸。咨询老师后,小林获悉废弃塑料的资源化回收是减少环境危害的最好方法。
(3)聚氯乙烯的生产需要用到氯气。工业上获取氯气的方法是电解饱和食盐水,发生反应的化学方程式为: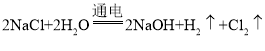 。某工厂需生产14.2t氯气(Cl2),至少需要氯化钠的质量为多少吨?____________(请写出计算过程)。
。某工厂需生产14.2t氯气(Cl2),至少需要氯化钠的质量为多少吨?____________(请写出计算过程)。
【答案】白色污染 H2O NaOH +HCl = NaCl + H2O 碱 NaCl、Na2CO3 产生白色沉淀,溶液仍为红色 向吸收液中加入适量的盐酸,至溶液恰好由红色变成无色 23.4t(详见解析)
【解析】
(1)购物袋等塑料制品的大量使用,可能会造成的一种环境污染是不可降解的速率引起的白色污染;
(2)①聚氯乙烯完全燃烧的化学方程式如下: ,
,
原子种类 | C | O | Cl | H |
反应物中原子个数 | 4n | 10n | 2n | 6n |
已知生成物中原子个数 | 4n | 8n | 2n | 2n |
差值(2nX) | 0 | 2n | 0 | 4n |
X的化学式 | H2O | |||
则X的化学式为H2O;
②将完全燃烧后的产物,全部通入到一定量的NaOH溶液中,得到吸收液,氢氧化钠溶液吸收氯化氢的化学反应是氢氧化钠和氯化氢生成氯化钠和水,方程式为NaOH +HCl = NaCl + H2O;
③【进行实验1】酚酞溶液遇碱性溶液显红色。取吸收液少许置于试管中,滴加2~3滴无色酚酞试液,发现酚酞变红色,说明溶液呈碱性;
[猜想]氯化氢先与氢氧化钠反应生成氯化钠和水,二氧化碳后与氢氧化钠反应碳酸钠、二氧化碳和水,所以反应后溶液中一定有NaCl,当氢氧化钠溶液足量时,二氧化碳和氢氧化钠反应生成碳酸钠,猜想2:NaCl、Na2CO3;
[进行实验2]碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,氯化氢、碳酸氢钠和氯化钙不反应,向实验1所得溶液中,加入过量的CaCl2溶液,将碳酸钠转化成氯化钠,由“猜想1正确”可知,溶液中还有呈碱性的氢氧化钠,故小林观察到产生白色沉淀,溶液仍为红色;
[交流反思]碳酸钠或碳酸氢钠,氢氧化钠都与盐酸反应生成氯化钠,实验结束后,小林对吸收液进行无害化处理,其方案是向吸收液中加入适量的盐酸,至溶液恰好由红色变成无色;
(3)设生产14.2t氯气(Cl2),至少需要氯化钠的质量为x

![]() x=23.4t
x=23.4t

【题目】研究气体的制备及相关气体的性质。

(1)写出实验室用过氧化氢溶液制取氧气的化学方程式_________。
(2)写出实验室用石灰石与稀盐酸反应制取二氧化碳的化学方程式________。
(3)某同学为了便于加入液体药品,在上述装置的橡胶塞上添加了一个注射器,该同学发现,这样做的优点还有_______(写出其中一点)。
(4)实验室里制取气体的一般思路和方法:
①选择适当的反应,包括_________;
②选择合适的________;
③验证所制得的气体。
(5)请设计实验验证制得的氧气和二氧化碳气体,并完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
______ | ______ | ______ |
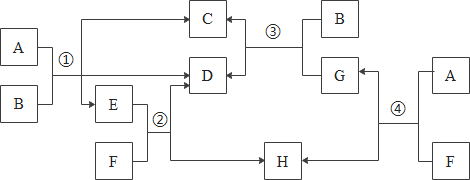
【题目】化学兴趣小组的同学在探究碱的化学性质时,完成了如图1所示的实验。

请你完成下列问题:
(1)第一组同学在向A中加入一定量的稀盐酸后,发现A中溶液仍然呈红色,则反应后溶液中的溶质是_____(酚酞除外,用化学式表示)。
(2)第二组同学做完A实验后溶液呈无色,用微观理论解释A中溶液变为无色的反应的实质是_____。
(3)第三组同学做B实验用于确认二氧化碳与氢氧化钠能发生化学反应(实验前K1、K2均处于关闭状态)。B实验全过程的操作及现象如表:
步骤 | 现象 |
第一步:打开_____,液体流下后,快速使其恢复关闭状态。 | 气球膨胀 |
第二步:_____ | 气球又收缩至原来状态 |
请写出导致气球膨胀的化学反应方程式_____。
(4)实验结束后,小军将以上同学做的A、B两个实验的废液均倒入同一个大烧杯中,观察到混合后的废液呈红色,由此产生疑问:
[提出问题]大烧杯的废液中含有哪些溶质?(酚酞除外)
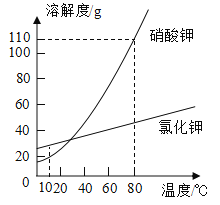
[查阅资料]氯化钙溶液呈中性,![]()
[实验验证]取一定量的废液,逐滴加入氯化钙溶液,如图2为同学们根据部分实验现象绘制的关系曲线。
[实验结论]如果观察到的现象只有沉淀产生,溶液仍然为红色,则废液中的溶质为(填化学式)_____;如果观察到有沉淀产生,溶液由红色变为无色,则废液中的溶质为(填化学式)_____。