题目内容
【题目】I、如图测所示,弹簧秤下挂着一重物A,烧杯中盛有溶液B,试根据要求回答下列问题:
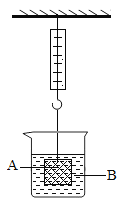
(1)若A为铁块,B为稀硫酸,则将A放入B中,过一会儿,弹簧秤的读数将(填 “变大”、“变小”或“不变”,下同)____;
(2)若A为铁块,B为硫酸铜溶液,则将A放人B中,过一会儿,弹簧秤的读数将______。
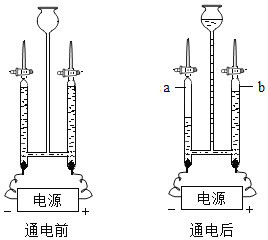
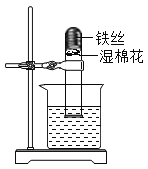
II、(1)如图所示,试管底部有螺旋状的光亮的铁丝,把试管倒插入水中,放置一周后,观察到铁丝表面有______生成,试管内的水面将_______,产生以上现象的原因是_______。
(2)某废液中含有HCl、FeCl2和CuCl2,要从中全部回收金属铜。某化学兴趣小组的同学先加入过量的铁粉,充分反应后过滤,滤渣中含有_______,如果想用化学方法继续实验得到金属铜,请写出简要步骤(包括加入试剂和操作方法)______
(3)现有铁片、铜片、硝酸汞溶液和盐酸几种物质,预确定Fe、Cu、Hg、H的活动顺序,有如下三种方案:
A Fe+HCl;Hg(NO3)2+Fe;Cu + HCl B Fe + HCl;Cu+HCl;Cu+Hg(NO3)2
C Fe+HCl;Fe +Hg(NO3)2;Cu+Hg(NO3)2
试评价这三种方案:①最差的方案是______,理由是_______;
②最好的方案是______,理由是_____。
【答案】变小 变大 铁锈 上升 铁与氧气、水等物质反应使试管内压强减小 铁和铜 加入适量盐酸(或稀硫酸、可溶性铜盐溶液),充分反应后过滤、洗涤、干燥 C Fe、Cu的活动性顺序不能确定,Cu、H的活动性顺序不能确定,Hg、H的活动性顺序不能确定 B 能将Fe、H、Cu、Hg的活动性顺序确定下来
【解析】
I、(1)若A为铁块,B为稀硫酸,则将A放入B中时铁与硫酸反应使溶液的溶质变成了硫酸亚铁,溶液的溶质质量分数变大,密度增加。浮力变大,则弹簧秤的读数将变小。
(2)若A为铁块,B为硫酸铜溶液,则将A放入B中,铁置换出铜,铜依附在铁表面,铜比铁相对原子质量大,故铁块重量增加,读数变大。
故答案为:变小;变大。
II、(1)试管内的铁丝与氧气和水充分接触,容易生锈.铁生锈的过程中铁与O2、水等物质反应,使试管内压强减小,从而使得水面上升.
故填:铁锈;上升;铁与氧气、水等物质反应使试管内压强减小.
(2)在金属活动性顺序中,铁排在铜的前面,可以与氯化铜发生置换反应生成铜,由于铁过量,故过滤后得到的滤渣中含有铜和铁两种物质.要除去其中的铁而获得纯净的铜,可以加入适量的酸除去铁或者是可溶性的铜盐将铁转化为铜,再过滤、洗涤、干燥.
故填:铁和铜;加入适量盐酸(或稀硫酸、可溶性铜盐溶液),充分反应后过滤、洗涤、干燥.
(3)根据各物质之间的反应,A方案可证明Fe>H,Fe>Hg,H>Cu,但Hg和H的顺序不能确定;B方案可证明Fe>H,H>Cu,Cu>Hg,即Fe>H>Cu>Hg;C方案可证明Fe>H,Fe>Hg,Cu>Hg,但Fe、Cu的活动性顺序不能确定,Cu、H的活动性顺序不能确定,Hg、H的活动性顺序不能确定;
故答案为:(1)C;Fe、Cu的活动性顺序不能确定,Cu、H的活动性顺序不能确定,Hg、H的活动性顺序不能确定
(2)B;能将Fe、H、Cu、Hg的活动性顺序确定下来。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案【题目】大理石广泛存在于自然界,某种大理石除主要成分![]() 外,还有少量的硫化钙。甲和乙两位同学用这种大理石和稀盐酸反应分别并展以下探究。
外,还有少量的硫化钙。甲和乙两位同学用这种大理石和稀盐酸反应分别并展以下探究。
(查阅资料)资料一:在常温下,测的浓度均为a%的下列5种溶液的pH大小情况:
溶质 |
|
|
|
|
|
pH | 小→大 | ||||
A ![]()
B ![]()
C ![]()
D ![]()
资料二:常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰
(实验探究)甲同学为了得到纯净的二氧化碳,设计了如下装置,请你

(1)制备的![]() 气体中,可能含有的杂质是___________;
气体中,可能含有的杂质是___________;
(2)上述装置中,A是_______溶液,饱和NaHCO3溶液可以吸收____;
(3)上述装置中,B物质可能是___________(写名称);
(4)用这个实验得到的气体测定![]() 的相对分子质量,如果B物质失效,测定结果_______(填“偏高”、“偏低”或“不受影响”);
的相对分子质量,如果B物质失效,测定结果_______(填“偏高”、“偏低”或“不受影响”);
(5)乙同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
实验步骤 | I.将适量盐酸加入烧杯中并称重 | II.称取少量大理石样品加入烧杯中,使之与过量稀盐酸反应 | III.待反应完全后,称重 |
实验图示 |
| ||
实验数据 | 烧杯和盐酸的质量为100.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
乙同学通过分析计算,得出结论:该实验中生成的二氧化碳的质量是4.4g,大理石样品纯度为83.3%。请你评价他的结论是否正确________(填“正确”或“错误”,并简述理由) __________。
【题目】某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,俊充分反应,实验数据如下:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
求:(1)黄铜样品中锌的质量分数____;(写出计算步骤,下同)
(2)完全反应后产生氢气的质量_____;
(3)所用稀硫酸的质量分数____。