题目内容
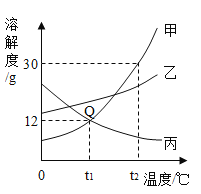
【题目】现有一定质量的碳酸钠溶液与稀盐酸恰好完全反应,其反应的图象如图所示
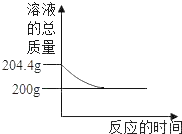
(1)求反应生成二氧化碳_____g
(2)求反应后所得溶液中的溶质质量分数_____?(写出计算过程)
【答案】4.4 5.85%
【解析】
碳酸钠与稀盐酸反应放出二氧化碳,因此完全反应前后烧杯内混合物的质量差即为放出二氧化碳气体的质量;根据反应的化学方程式,由生成二氧化碳气体的质量计算出样品中碳酸钠的质量以及出生成氯化钠的质量,同时依据碳酸钠的质量可求出原混合物中氯化钠的质量,据此可计算所得溶液的溶质质量分数。
解:(1)根据质量守恒定律,生成二氧化碳的质量为204.4g﹣200g=4.4g;
(2)设反应中生成NaCl的质量为x,
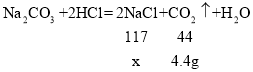
![]()
x=11.7g;
反应后所得NaCl溶液的质量分数为:![]() ×100%=5.85%;
×100%=5.85%;
答:反应所得溶液中溶质的质量分数5.85%。

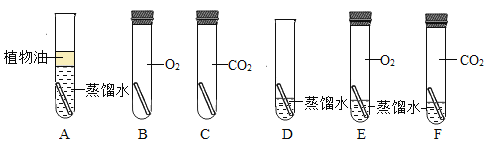
【题目】向碳酸氢镁[Mg(HCO3)2]溶液中加入一定量NaOH溶液,出现白色沉淀。某化学兴趣小组同学对该白色沉淀作如下探究:
(查阅资料)I.Mg(OH)2是一种难溶于水的白色固体,MgCO3是一种微溶于水的白色固体。
Ⅱ.Mg(OH)2、MgCO3受热均易分解,分别生成对应的两种氧化物。
Ⅲ.无水硫酸铜是一种白色固体,遇水变蓝。
(作出猜想)猜想一:只有Mg(OH)2;猜想二:只有MgCO3:;猜想三:_____。
(实验1)
步骤 | 实验操作 | 实验现象 | 实验结论 |
步骤1 | 取适量白色固体,加入足量的稀盐酸 | 有气泡产生 | 猜想_____不成立 |
步骤2 | 另取适量白色固体,充分加热,将产生的气体通入盛有无水硫酸铜的U形管 | _____ | 猜想二不成立 |
小张查阅资料得知上述固体是碱式碳酸镁[XMgCO3yMg(OH)23H2O],它不溶于水,受热易分解。
(实验2)
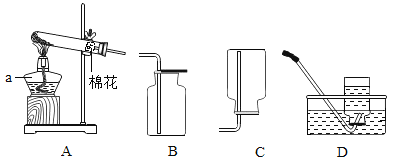
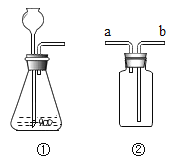
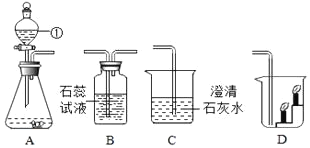
为进一步确定白色固体的组成,小张取一定量白色固体,按下图装置加热至固体质量不再改变,并测定各生成物的质量。
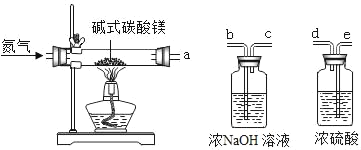
(1)反应结東后若没有继续通一会儿氮气就直接称量洗气瓶的质量,则测得的气体质量将_____(填:“偏大”、“偏小”或“不变”)
(2)为测定各生成物的质量,导管口的连接顺序为a→_____,_____→_____(填字母)。
(3)实验数据:加热完全后剩余固体质量3.20g;浓NaOH溶液增重2.64g;浓硫酸增重1.44g则:x:y=_____。
(拓展延伸)
碱式碳酸镁可作阻燃剂,其可能的原因是_____(选填字母)。
a生成的固体覆盖在燃烧物表面,隔绝氧气
b分解时吸热,使温度难以达到可燃物的着火点
c生成的气体降低了可燃物周围的氧气浓度