题目内容
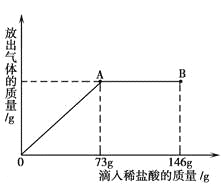
【题目】在一烧杯中盛有20.4g Na2CO3和NaCl 组成的固体混合物。向其中逐渐滴加溶质质量分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
(1) 当滴加稀盐酸至图中B点时,烧杯中溶液的pH ▲ 7(填>、=、<)。
(2) 原混合物中碳酸钠的质量。
(3) 当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)。
【答案】(1)< (2)10.6g (3)24.2%
【解析】
试题(1)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,由图可知,A点时表示碳酸钠与盐酸恰好完全反应,B点表示的是盐酸过量,此时溶液的PH<7;
(2)由图可知当盐酸与碳酸钠恰好完全反应时消耗的盐酸中溶质的质量=73g×10%=7.3g,利用化学方程式碳酸钠与盐酸反应的质量比即可计算出碳酸钠的质量;
设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y,生成的二氧化碳的质量为z,那么:
Na2CO3 + 2HCl ="=" 2NaCl + H2O + CO2↑
106 73 117 44
x 7.3g y z
106/x =73/7.3g 117/y =73/7.3g 44/z =73/7.3g
X=10.6g y=11.7g z=4.4g
(3)烧杯中溶质的质量包括两部分:11.7g+(20.4g-10.6g)=21.5g
烧杯中溶液的质量=20.4g+73g-4.4g=89g
那么溶质的质量分数=21.5g/89g ×100%=24.2%
答:略

练习册系列答案
相关题目