��Ŀ����
����Ŀ����ѧ������������ϢϢ��أ������û�ѧ֪ʶ�ش��������⣺
��1������ˮ����ˮ�����������������������أ�K2FeO4����һ�ָ�Ч����������������Ԫ�صĻ��ϼ�Ϊ____��
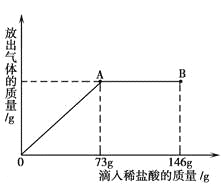
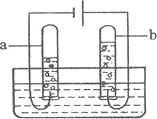
��2����ͼ��ˮͨ��ֽ��ʾ��ͼ����ʵ������У��Թ�b�в�����������______��a��b������������Ϊ__________��д���÷�Ӧ�Ļ�ѧ����ʽ�� ________,�����Ӧ˵��ˮ����___________��ɵġ�
��3������Σ��Ʒ��ը�¹�����һ�ֽе�ʯ��CaC2�������ʣ���ˮ��Ӧ������Ȳ��C2H2��������������ƣ���ѧ��Ӧ����ʽΪ_________________________��
���𰸡�+6 ���� 2:1 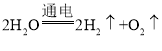 ����Ԫ��
����Ԫ�� ![]()
��������
��1��������أ�K2FeO4���м�Ԫ����+1�ۣ���Ԫ����-2�ۣ����ݻ����ﻯ�ϼ۴�����Ϊ�㣬����Ԫ�ػ��ϼ�Ϊx����![]() ��x=+6�����+6��
��x=+6�����+6��
��2��ˮͨ������У����������������������ԼΪ2:1�����Թ�b�в�������������������Ӧ�Ļ�ѧ����ʽ��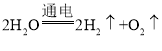 ,�����Ӧ˵��ˮ��������Ԫ����ɵġ����������2:1��
,�����Ӧ˵��ˮ��������Ԫ����ɵġ����������2:1��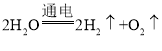 ������Ԫ��
������Ԫ��
��3����ʯ��CaC2����ˮ��Ӧ������Ȳ��C2H2��������������ƣ���ѧ��Ӧ����ʽΪ![]() �����
�����![]() ��
��

 С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д� �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д� �¸��̵�ѧϵ�д�
�¸��̵�ѧϵ�д� ����ͬѧһ����ʦȫ�źþ�ϵ�д�
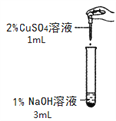
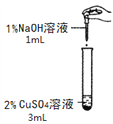
����ͬѧһ����ʦȫ�źþ�ϵ�д�����Ŀ����һ�λ�ѧʵ���У�����ͬѧ�����������ͭ��Һ������������Һ��Ӧ��ʵ�飬���۲쵽�˲�ͬ��ʵ������
��ʵ��һ��
ʵ���� | ���� | ���� |
ʵ����� |
|
|
ʵ������ | ������ɫ���� | ��������ɫ���� |
����֪��ɫ������������ͭ��д��������ɫ�����Ļ�ѧ����ʽ______��
��������⡿�������������ɫ�����ijɷ���ʲô�أ�
���������ϡ�
��ʽ����ͭ����ɫ���壬��ˮ���ܽ�ȼ�С��������ϡ����Һ��
��ʽ����ͭ����ɲ��̶���һ�����Cu2(OH)2SO4��ʾ��
����������衿����ɫ�����Ǽ�ʽ����ͭ��
��ʵ�����
ʵ�鲽�� | ��Ҫʵ����� | ������ |
�� | ȡ����ʵ���Ļ������� | �õ�����ɫ���� |
�� | ȡ����ɫ������������ˮϴ�Ӷ�� | ���������� |
�� | �����һ��ϴ��Һ�еμ�BaCl2��Һ | �������� |
�� | ȡϴ�Ӻ������ɫ�������Թ��У��μ�ϡ���� | ����ȫ���ܽ⣬�õ�����ɫ��Һ |
�� | ȡ��������ɫ��Һ���Թ��У��μ��Լ�X | ������ɫ���� |
ʵ����ۣ�����ɫ�����Ǽ�ʽ����ͭ | ||
����������ۡ�
�Ʋ���۵�ʵ��Ŀ����______��
�Dz�����е�ϡ����______��ѡ��ܡ����ܡ�����ϡ������档
�Ȳ�����еμӵ��Լ�X��______��
����˼�����ۡ�
�ɼ���ͬѧ�ڱ���ʵ��Ļ����Ͻ�һ��������ʵ�飺
�ٹ��ˣ�ȡ��ɫ�������Թ��У�
�ڵμ�______��������ɫ��Ϊ����ɫ��
���ظ�ʵ����еIJ���١��ݡ�
��ʵ����֤��������ͭҲ����ת��Ϊ��ʽ����ͭ���˷�Ӧ�Ļ�ѧ����ʽΪ______��
������ͬѧ��Ϊ���Լ���ԭ��ʵ��Ļ����ϣ������μ�______�����Խ���ʽ����ͭת��Ϊ������ͭ��ͨ��ʵ�飬Ҳ��֤�����ǵIJ��롣
��Ϊ��ȷ������������Һ������ͭ��Һ��Ӧ����������ͭ��ʵ��Ĺؼ���______��