��Ŀ����
����Ŀ���ڹ������£�AgNO3 �ɷֽ�Ϊ Ag��O2 ��ij�ֵ��������� X��ȡһ��������AgNO3�����ֹ��գ���÷�Ӧ������ Ag��O2��X �������ֱ�Ϊ 10.8g��mg��4.6g������˵����ȷ���ǣ�������
��AgNO3����Ӧ�ܷⱣ������ɫϸ��ƿ��
��m��1.6
��X�Ļ�ѧʽΪNO2
�ܸ÷�Ӧ����ʽ��Ag��O2�Ļ�ѧ������֮��Ϊ3��2
A.�ڢ�B.�ۢ�C.�٢ڢ�D.�ڢۢ�
���𰸡�A
��������
��AgNO3��������ֽ⣬Ӧ�ܷⱣ������ɫϸ��ƿ�У���ѡ��˵������ȷ��
����Ԫ��������10.8g����������������10.8g��![]() ��17g��m��17g��10.8g��4.6g��1.6g����ѡ��˵����ȷ��
��17g��m��17g��10.8g��4.6g��1.6g����ѡ��˵����ȷ��
�۵�������������Ԫ��������17g��![]() ��1.6g��3.2g����Ԫ��������17g��
��1.6g��3.2g����Ԫ��������17g��![]() ��1.4g��X�е�ԭ�ӡ���ԭ�Ӹ����ȣ�
��1.4g��X�е�ԭ�ӡ���ԭ�Ӹ����ȣ�![]() ��1��2�����X�Ļ�ѧʽΪNO2����ѡ��˵����ȷ��
��1��2�����X�Ļ�ѧʽΪNO2����ѡ��˵����ȷ��
�ܸ÷�Ӧ����ʽ��Ag��O2�Ļ�ѧ������֮��Ϊ��![]() ��2��1����ѡ��˵������ȷ��
��2��1����ѡ��˵������ȷ��
��ѡA��

����Ŀ��ijͬѧѧϰCO2����ȡ������ʱ�����������ʵ��̽�����ݡ���Ҫ����⡣
��1����ͬʵ��Է�Ӧ�����в�ͬҪ�����ṩ����ѡѡ����ѡ�����ѡ����д�±���
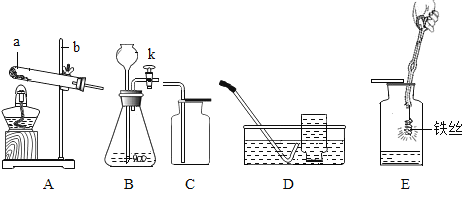
��ѡ���Ʒ�Ӧ���ʵķ������ٷ�Ӧ���Ũ�� �ڷ�Ӧ���״̬ �۴���
��ѡ�Լ���Aϡ���� BŨ���� C��״ʯ��ʯ D̼������Һ E��ĩ״ʯ��ʯ F��������G.H2O2��Һ
ʵ������ | ��ѡ�õ�����Լ� | �������ʵķ��� |
����������������ʾ���� | G��F | �� |
CO2��ʵ�����Ʒ� | A��_______ | ________ |
��2��Ϊ̽��SO2��CO2��������ͬ�����������ʵ�飺��ˮ����ע��һ�����������ˮ���������еμӼ����Լ�X��Ȼ�ֱ���SO2��CO2����������Թ�ͬʱ������ˮ���У�Ƭ�̺�ʵ����������ͼ��ʾ���Թ�����Һ��ɺ�ɫ������������ʵ�鱨�棺
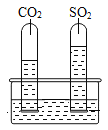
��SO2��CO2һ��������ˮ���ܽ���SO2_____CO2(��������������������=��)��
��SO2��CO2һ����ˮ��Ӧ���������������Ե����ʣ�X��______��
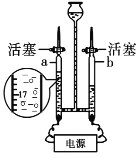
����Ŀ��ij��ѧ��ȤС��Ϊ����֤�����غ㶨�ɣ�����þ���ڿ�����ȼ�յ�ʵ�顣
��1��С������ȼ�ղ�����������ڷ�Ӧ��þ������������Ϊ�����Ӧ�����������غ㶨�ɣ���_____���ͬ�⡱��ͬ�⡱��С���Ĺ۵㣬��Ϊ_____��
��2��С�찴��ͼװ�øĽ�ʵ�飬��֤�������غ㶨�ɣ�ȴ���ֲ����л���������ɫ���塣
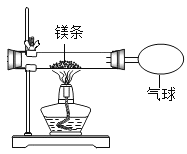
��������⣩��ɫ������ʲô�أ�
���������ϣ�������þΪ��ɫ���壻
��þ���뵪�����ҷ�Ӧ���ɻ�ɫ�ĵ���þ��Mg3N2�����壬д��������þ��Ӧ�Ļ�ѧ����ʽ_____��
�۵���þ����ˮ���ҷ�Ӧ������������������ʹʪ��ĺ�ɫʯ����ֽ������
��ʵ�������
�������� | ʵ������ | ʵ����� |
_____ | _____ | ��ɫ����ΪMg3N2 |
���������룩��ɫ������Mg3N2
��ʵ��̽���������ʵ�飬��֤����
����˼�뽻����������N2�ĺ���Զ����O2�ĺ�������þ���ڿ�����ȼ�����ɵ�MgOȴԶ����Mg3N2��Ϊʲô�أ�����������Ľ���_____��
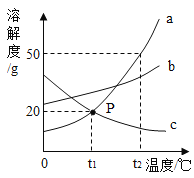
����Ŀ��С���������������Һʱ�õ��±����ݣ��ݴ˷�������˵����ȷ���ǣ�������
��� | �¶�/�� | ˮ������/�� | ��������ص�����/�� | ������Һ������/�� |
�� | 10 | 100 | 40 | 120.9 |
�� | 60 | 100 | 40 | 140 |
A.10��ʱ����ص��ܽ��Ϊ40��
B.��������Һһ����60��ʱ����صı�����Һ
C.��ͨ�����Ƚ�����ʣ�������ȫ���ܽ⣬����Һ�������������������ǰ����һ��
D.������������Һ������10�棬����Һ�����������������С