题目内容
【题目】小金在配制硝酸钾溶液时得到下表数据,据此分析以下说法正确的是( )
序号 | 温度/℃ | 水的质量/克 | 加入硝酸钾的质量/克 | 所得溶液的质量/克 |
① | 10 | 100 | 40 | 120.9 |
② | 60 | 100 | 40 | 140 |
A.10℃时硝酸钾的溶解度为40克
B.②所得溶液一定是60℃时硝酸钾的饱和溶液
C.若通过加热将①中剩余硝酸钾全部溶解,则溶液的溶质质量分数与加热前保持一致
D.若将②所得溶液降温至10℃,则溶液的溶质质量分数会变小
【答案】D
【解析】
A、10℃时,在100g的水中,加入40g的硝酸钾,形成溶液的质量为120.9g,所以硝酸钾的溶解度为20.9克,此选项错误;
B、②中的固体全部溶解,所得溶液不能说就是60℃时硝酸钾的饱和溶液,此选项错误;
C、若通过加热将①中剩余硝酸钾全部溶解,溶质质量增大,则溶液的溶质质量分数增大,此选项错误;
D、②所得溶液溶质质量分数为:![]() =28.6%,降温至10℃,溶质质量分数变为:
=28.6%,降温至10℃,溶质质量分数变为:![]() =17.3%,溶液的溶质质量分数变小,此选项正确。
=17.3%,溶液的溶质质量分数变小,此选项正确。
故选D。

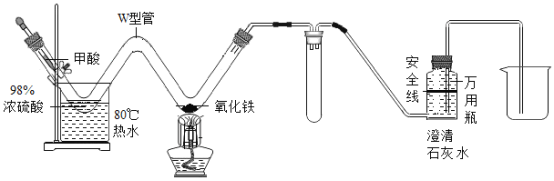
【题目】某化学小组探究炼铁的反应原理。
(一)利用图装置回答问题(假设赤铁矿粉样品中的Fe2O3完全反应,赤铁矿中杂质不参与反应):
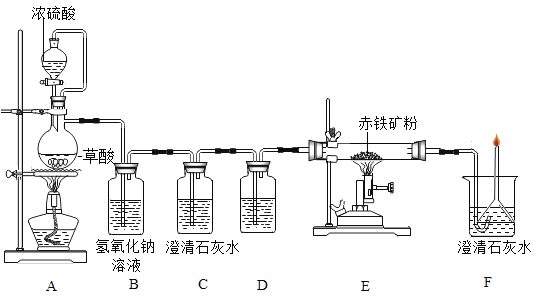
(1)A装置的作用是制取一氧化碳,反应的化学方程式为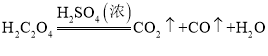 。根据反应装置判断,化学方程式中还缺少的条件是___________________。
。根据反应装置判断,化学方程式中还缺少的条件是___________________。
(2)C装置的作用是______,D装置中药品的名称是________,E装置中发生反应的化学方程式为________,F处将尾气燃烧掉的目的是______。
(3)实验中记录的数据如下表,据此计算赤铁矿中氧化铁的质量分数为________。
玻璃管质量 | 玻璃管和药品反应前质量 | 玻璃管和药品反应后质量 |
65.6g | 75.6g | 73.2g |
(4)有同学提出可以根据F装置中增加的质量来计算赤铁矿中氧化铁的质量,你同意此看法吗?
说出你的观点和理由是_______。
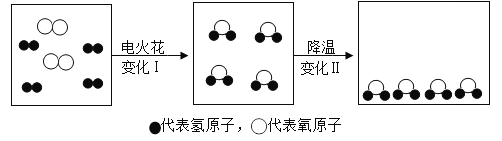
(二)利用图装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置和尾气处理装置略,所用固体药品为纯净物)。
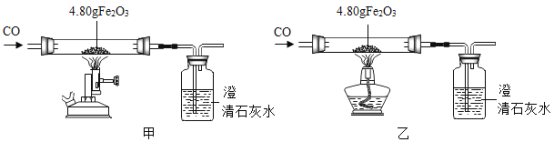
(1)反应过程中观察到,甲、乙两组的澄清石灰水均变浑浊,集气瓶中发生反应的化学方程式为________。
(2)完全反应后,甲、乙两组的生成物均为黑色粉末,分别用两组的生成物进行以下实验:
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 称量黑色粉末质量/g | m1 | m2 |
2 | 取黑色粉末,用磁铁吸引 | 全部被吸引 | 全部被吸引 |
3 | 取黑色粉末,加入足量CuSO4溶液 | 黑色粉末溶解,有红色物质生成 | 无明显现象 |
(注:铁的氧化物中,只有Fe3O4能被磁铁吸引)
①甲组的黑色粉末与CuSO4溶液反应的化学方程式是_____。
②小明同学查阅资料后发现Fe3O4在常温下不与CuSO4溶液反应,故猜想乙组的生成物为Fe3O4。
小丽提出不同意见:假设乙组黑色粉末中除了有Fe3O4,还可能含有少量铁粉,铁粉的含量低,与硫酸铜溶液反应也可能无明显现象。
了进一步确定乙组生成物成分,小组同学提出,如果m2恰好为______________g,则小明的猜想正确,如果m2_____________________(填“大于”或“小于”)该质量,则乙组生成物中还含有少量铁粉。
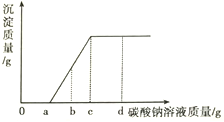
【题目】复习硬水、软水及其自来水的软化知识时,某小组的同学们进行了如下探究。
知识回顾: (1)溶有较多可溶性钙镁化合物的水,叫硬水。
(2)硬水软化的原理是设法降低水中可溶性钙镁化合物的含量。
任务一:当地自来水是否为硬水?
(实验准备)取一定量当地自来水于烧杯中,滴加几滴稀盐酸酸化。
[进行实验]小组同学设计检验Mg2+、Ca2+实验方案如下:
实验步骤 | 实验操作 | 实验现象 |
I | 取少量烧杯中溶液于试管中,滴加足量的NaOH溶液 | ______ |
II | 取步骤I上层清液于另一试管中,滴加几滴_____ | 产生白色沉淀 |
(实验结论)当地自来水为硬水
(交流总结)实验步骤I、Ⅱ中发生反应的微观实质是_____(答出一点)。
任务二:自来水在煮沸后有水垢生成,水垢的主要成分是什么?
(猜想与假设)水垢中可能有碳酸钙。
(实验探究)小明收集热水壶内壁上的少量水垢于试管中,滴加_____,观察到有气泡产生,说明水垢中有碳酸钙。
(反思评价)
(1)除去水垢发生反应的化学方程式为_____;
(2)小红认为小明实验设计不合理,还要增加一个证明气体成分的实验,该设计是_____。
任务三:
(联系实际)小组同学走访许多工厂和家庭,了解到很多硬水软化的方法,并对硬水的危害有了更多的认识,联系实际,硬水软化的一种方法是_____,硬水的另一种危害是_____。