题目内容
【题目】A—E是初中化学中常见的五种物质,它们之间的关系如图所示(各字母代表一种物质,“→”表示物质间的转化关系,部分反应物、生成物及反应条件未标出)。其中,反应①②③分别是三种不同的基本反应类型,且反应③中固体由红色变成黑色。
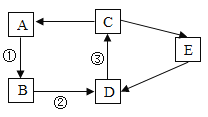
(1)写出E的化学式:_____;
(2)写出A→B化学方程式:_____。
【答案】![]() 或
或![]() 或
或![]()

【解析】
反应①②③分别是三种不同的基本反应类型,反应③中固体由红色变成黑色,所以D是铜, C是氧化铜,反应①②③分别是三种不同的基本反应类型,所以A是水,B是氢气,E是可溶性铜盐,可以是硫酸铜或氯化铜或硝酸铜,代入验证,推理正确。
(1)由分析可知,E的化学式:![]() 或
或![]() 或
或![]() ;
;
(2)A→B是水在通电下反应生成氢气和氧气,反应的化学方程为: 。
。

 名校课堂系列答案
名校课堂系列答案【题目】电影《我和我的祖国》中有这样一则片段:开国大典前夜, 升旗试验出了问题,旗杆顶部的阻断球因锈蚀变脆而折断,为保证当天升 旗成功,采用焊接方式换上新的不锈钢阻断球,最终升旗仪式完美无缺。

(一)阻断球是常见的铁制品,工业上常用设备高炉来炼铁,主要原料是 焦炭、赤铁矿石(主要含 Fe2O3)、石灰石、空气等,主要反应过程如下:

请回答:
(1)将炼出的“铁”加足量盐酸,充分反应后,总有黑色物质剩余,该黑色物质为________填 化学式);
(2)反应②的化学方程式为_____,该反应所属的基本反应类型为_____。
(二)金属的锈蚀及防护
(1)铁质阻断球的生锈,实际上是铁与_______、_____________共同作用的结果。铁锈的颜色是______;下列情况下铁制品最易生锈的是______(填序号).
a 潮湿空气中 b 干燥空气中 c 部分浸入食盐水中
(2)生活中的铁制品琳琅满目,铁还可以作铁锅利用了铁的_______性,请写出一种生活中防止铁锅生锈的方法:_______。
(3)金属铝比铁活泼,却具有很好的抗腐蚀性,原因是_____________ (用方程式表示)
(三)铁锈组成分析测定
(查阅资料)铁锈成分复杂,化学式可简单表示为 Fe2O3nH2O,在加热时会分步反应,首 先失去结晶水,其反应可表示为 Fe2O3nH2O![]() Fe2O3+nH2O。浓硫酸可以吸水,碱石灰 可以吸收水和二氧化碳。
Fe2O3+nH2O。浓硫酸可以吸水,碱石灰 可以吸收水和二氧化碳。
(提出问题)铁锈(Fe2O3nH2O)中 n 的值等于多少呢?
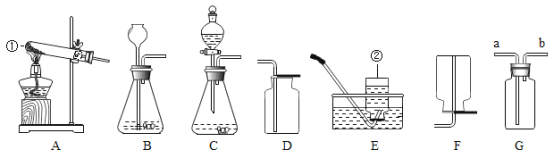
(问题探究)为了探究铁锈(Fe2O3nH2O)的组成,称取 30.0g 部分生锈的铁粉样品,样品中仅含铁和 Fe2O3nH2O,按如图 2 所示装置进行实验。
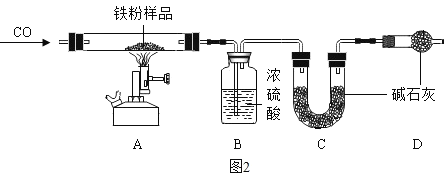
(1)为了保证实验安全,实验开始时应先通 CO,目的是_______;
(2)反应结束后还需持续通 CO,除了防止铁氧化以外,还有_______ 的目的。
(3)实验结束后,A 中玻璃管内出现的现象是_______ ;
(4)请指出该装置中有一处明显不足_______ ;
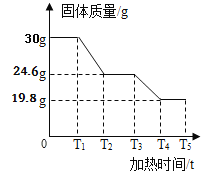
(数据处理)图 3 是加热时间和 A 中固体质量关系图象,下表是 B、C 中质量不再变化时 B中浓硫酸、C 中碱石灰装置质量变化情况。
反应前(g) | 反应后(g) | |
B | 100 | 105.4 |
C | 150.0 | 163.2 |
(5)完全反应产生的二氧化碳质量为_______ ;铁锈(Fe2O3nH2O)中 n 的值是______;
(6)写出 T3-T4 时间段所发生的化学方程式_______
(7)计算 30g 样品中单质铁的质量分数_______。(写出计算过程,结果保留到 0.1%)