题目内容
【题目】向HCl和FeCl3的混合溶液中,不断加入NaOH溶液,下图曲线正确的是( )
A.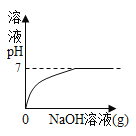
B.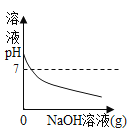
C.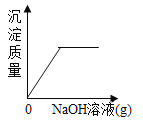
D.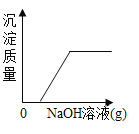
【答案】D
【解析】
向HCl和FeCl3的混合溶液中,不断加入NaOH溶液,氢氧化钠先与盐酸反应生成氯化钠和水,导致溶液的酸性逐渐减弱,pH逐渐变大,氢氧化钠与盐酸恰好完全反应时溶液的pH=7。当氢氧化钠与盐酸反应后,继续滴加氢氧化钠,氢氧化钠与氯化铁反应生成氢氧化铁沉淀和氯化钠,即要一段时间后才会产生沉淀。
A、开始时溶液呈酸性,氢氧化钠先与盐酸反应生成氯化钠和水,导致溶液的酸性逐渐减弱,pH逐渐变大,氢氧化钠与盐酸恰好完全反应时溶液的pH=7,氢氧化钠溶液与HCl和FeCl3全部反应后,继续加入氢氧化钠溶液,溶液的pH应该大于7,选项A错误;
B、开始时溶液呈酸性,pH<7,选项B错误;
C、氢氧化钠先与盐酸反应,再与氯化铁反应,故要一段时间后才会产生沉淀,选项C错误;
D、氢氧化钠溶液先与盐酸反应,再与氯化铁反应,故要一段时间后才会产生沉淀,氯化铁反应结束后,沉淀不再增加,选项D正确。故选D。

练习册系列答案
相关题目
【题目】某化学兴趣小组为了测定石灰石样品中碳酸钙的质量分数,将 200g 稀盐酸平均分成 4 等分,分别加入样品中,充分反应后称得生成气体质量,得到的实验数据如下:
第一次 | 第二次 | 第三次 | 第四次 | |
样品质量(g) | 5 | 10 | 15 | 20 |
稀盐酸质量(g) | 50 | 50 | 50 | 50 |
生成气体质量(g) | 1.76 | 3.52 | 4.4 | m |
(1)表中 m= 。
(2)第一次反应后所得溶液中的溶质是 (填化学式)。
(3)计算该石灰石样品中碳酸钙的质量分数 ?