题目内容
将148g氯化钙溶液与一定量的碳酸钠溶液混合,恰好完全反应.过滤后,得到20g沉淀和溶质质量分数10%的溶液.求:碳酸钠溶液中溶质质量分数是多少?
20%
解析试题分析:(1)设生成20g碳酸钙需要碳酸钠的质量为x,生成氯化钠的质量为y
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100 117
x 20g y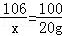
x=23.4g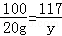
y=21.2g
生成的氯化钠溶液的质量=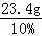 =234g
=234g
碳酸钠溶液的质量=234g+20g﹣148g=106g
碳酸钠溶液中溶质质量分数= =20%
=20%
答:碳酸钠溶液中溶质质量分数20%
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算..

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
某校化学兴趣小组同学用一瓶含有少量氯化钠的硫酸钠固体样品,进行如下图所示的实验。
已知:Na2SO4 + BaCl2 = BaSO4↓ + 2NaCl
请根据以上信息,计算反应后所得溶液中溶质的质量分数。
化学兴趣小组为了测定石灰石中碳酸钙的质量分数(杂质不溶于水,也不与盐酸反应).测得的数据如下:
| 实验组次 | 1 | 2 | 3 | 4 |
| 样品质量/g | 30 | 20 | 20 | 30 |
| 稀盐酸的质量/g | 50 | 50 | 100 | 100 |
| 产生气体的质量/g | 6.6 | 6.6 | 6.6 | m |
(1)m的值为多少?
(2)第 组实验恰好完全反应?
(3)该石灰石样品的纯度是多少?
 2CuSO4 + 2H2O)现有溶质的质量分数为10%的稀硫酸(其中含溶质98 g)与铜恰好完全反应,假设硫酸不和其他杂质反应,求反应后硫酸铜溶液中溶质的质量分数。(最后结果精确到0.1%)
2CuSO4 + 2H2O)现有溶质的质量分数为10%的稀硫酸(其中含溶质98 g)与铜恰好完全反应,假设硫酸不和其他杂质反应,求反应后硫酸铜溶液中溶质的质量分数。(最后结果精确到0.1%)