题目内容
据报道,化工生产中产生的含铜废料,在通入空气并加热的条件下,能与稀硫酸反应转化为硫酸铜。(2Cu + 2H2SO4 + O2 2CuSO4 + 2H2O)现有溶质的质量分数为10%的稀硫酸(其中含溶质98 g)与铜恰好完全反应,假设硫酸不和其他杂质反应,求反应后硫酸铜溶液中溶质的质量分数。(最后结果精确到0.1%)
2CuSO4 + 2H2O)现有溶质的质量分数为10%的稀硫酸(其中含溶质98 g)与铜恰好完全反应,假设硫酸不和其他杂质反应,求反应后硫酸铜溶液中溶质的质量分数。(最后结果精确到0.1%)
15.1%
解析试题分析:反应后硫酸铜溶液中溶质的质量分数等于溶质硫酸铜的质量除以反应后溶液的质量再乘以百分之一百。溶质硫酸铜的质量可利用化学方程式计算出来。
解:设生成的溶质硫酸铜的质量为X ,参加反应的铜的质量为y ,氧气的质量为z:
2Cu + 2H2SO4 + O2 =2CuSO4 + 2H2O
128 196 32 320
y 98g z X
196/320 = 98g/X 196/128 =98g/y 196/32 =98g/z
X=160g y =64g z =16g
反应后溶液的质量=" 64g" +16g +(98÷10%)=1060g
反应后硫酸铜溶液中溶质的质量分数=160g/1060g ×100% =15.1%
考点:有关溶质质量分数的计算

 培优三好生系列答案
培优三好生系列答案一瓶久置的氢氧化钠固体已经发生了变质,某研究小组为了探究氢氧化钠的变质纯度,作出如下猜想:猜想一、可能部分变质,固体是NaOH和Na2CO3的混合物;猜想二、可能全部变质,固体是Na2CO3。
(1)首先对固体的成分进行确定。取少量固体于试管中,加水充分溶解,先加入足量的BaCl2溶液,产生白色沉淀,静置后取上层溶液,再加入CuSO4溶液,产生蓝色絮状沉淀。根据实验现象,可判断 是正确的。
(2)称取10.6克该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
计算该样品中Na2CO3的质量分数。
(3)请你分析,一定质量的NaOH固体,变质前后与足量的稀盐酸反应,变质前生成NaCl
的量 (填“大于”、“等于”、或“小于”)变质后生成NaCl的量。
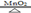 KCl + 3O2↑。现将 29.4g 氯酸钾与 5.6g 二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.4g。回答:
KCl + 3O2↑。现将 29.4g 氯酸钾与 5.6g 二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.4g。回答: