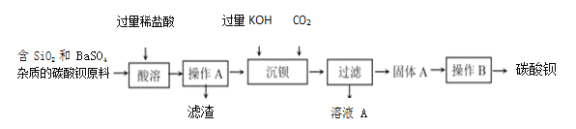
题目内容
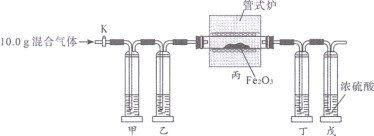
【题目】某化学兴趣小组欲测定一瓶过氧化氢溶液![]() 过氧化氢和水的混合物
过氧化氢和水的混合物![]() 中过氧化氢的质量,实验操作及相关数据如图所示:
中过氧化氢的质量,实验操作及相关数据如图所示:
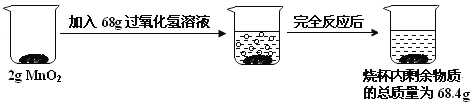
(1)生成氧气的质量______g,计算的依据是______
(2)这瓶过氧化氢溶液中过氧化氢的质量是_______?![]() 请根据方程式计算
请根据方程式计算![]()
【答案】1.6g 质量守恒定律 3.4g
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了氧气,所以可以求算氧气的质量,根据氧气的质量和对应的化学方程式求算过氧化氢溶液中![]() 的质量。根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
的质量。根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
根据质量守恒定律可知,反应前后物质的总质量不变,生成的氧气的质量为![]()
设过氧化氢的质量为x

68/32=x/1.6g
X=3.4g
答:(1)生成氧气的质量![]() ,计算的依据是质量守恒定律;
,计算的依据是质量守恒定律;
(2)过氧化氢溶液中![]() 的质量为
的质量为![]() 。
。

练习册系列答案
相关题目
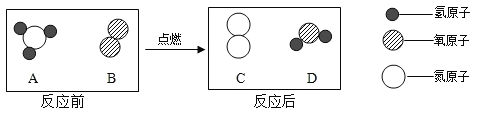
【题目】把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
物质 | A | B | C | D |
反应前质量 |
|
|
|
|
反应后质量 | 待测 |
| 0 |
|
下列说法正确的是![]()
A. 物质C一定是反应物,物质D可能是单质
B. 反应后密闭容器中A的质量为![]()
C. 反应过程中,物质B和物质D变化的质量比为87:36
D. 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1