题目内容
【题目】现有碳酸钠和金属单质锌的混合物,为测定其组成,取一定质量该混合物放于烧杯中,向烧杯中加入300g溶质质量分数为9.8%的稀硫酸,恰好完全反应,得到一定温度下的不饱和溶液318.8g,则下列判断正确的是( )
A.生成CO2的质量为4.4g
B.生成H2的质量为0.4g
C.混合物中碳酸钠的质量5.3g
D.混合物中单质锌的质量13g
【答案】ABD
【解析】
稀硫酸和碳酸钠反应生成硫酸钠、水和二氧化碳,和锌反应生成硫酸锌和氢气。
解:设碳酸钠质量为![]() ,锌质量为
,锌质量为![]() ,生成二氧化碳的质量为
,生成二氧化碳的质量为![]() ,生成氢气的质量为
,生成氢气的质量为![]() ,溶液增重质量△m=318.8g﹣300g=18.8g
,溶液增重质量△m=318.8g﹣300g=18.8g
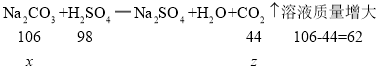
根据反应方程式可知,![]() g碳酸钠消耗硫酸的质量为
g碳酸钠消耗硫酸的质量为![]() ,溶液质量增大为
,溶液质量增大为![]() 。
。
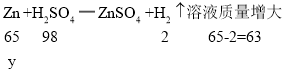
根据反应方程式可知,![]() g锌消耗硫酸的质量为
g锌消耗硫酸的质量为![]() ,溶液质量增大为
,溶液质量增大为![]() 。
。
![]() +
+![]() =300g×9.8%
=300g×9.8%
![]() +
+![]() =18.8g
=18.8g
![]() =10.6g
=10.6g
![]() =13g
=13g
则![]()
![]()
解得![]() =4.4g
=4.4g
![]() =0.4g
=0.4g
A、生成二氧化碳的质量为4.4g,故选项正确;
B、生成氢气的质量为0.4g,故选项正确;
C、混合物中碳酸钠的质量为10.6g,故选项错误;
D、混合物中单质锌的质量为13g,故选项正确。故选ABD。

 名校课堂系列答案
名校课堂系列答案【题目】金属及其化合物在生产生活中有广泛的应用。
(一)金属的应用和防护
(1)飞机的燃料是航空煤油,它主要是由____炼制的(填“石油”或“煤”)。
(2)铁生锈需要同时接触O2和____,请提出生活中铁制品防锈的一种方法____。
(3)特种钢中的Mn可以由MnO2和Al粉混合在高温下通过置换反应制得,该化学方程式为____。
(4)Mg(OH)2受热分解生成MgO,Mg(OH)2用作阻燃剂,其原理是____(填字母)。
A 分解吸热,降低环境温度 B MgO覆盖燃烧物,隔绝氧气
(二)制备还原性铁粉
实验室利用废铁屑(含少量Fe2O3)为原料制备还原性铁粉的流程如下:
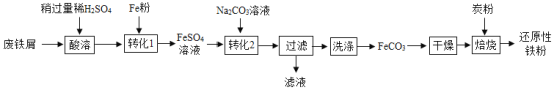
(1)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为____。
(2)检验FeCO3已洗净的方法:取最后一次洗涤后的滤液,先加入一定量稀盐酸,除去CO32-,再滴加____溶液,无明显现象。
(3)“干燥”发生转化:FeCO3 ![]() FeOOH+CO2,该转化的化学方程式为____。
FeOOH+CO2,该转化的化学方程式为____。
(4)“焙烧”前,应将炭粉与“干燥”所得固体均匀混合,目的是____。
(三)测定还原性铁粉的组成
还原性铁粉中含有少量FexCy,小组同学在老师的指导下进行以下实验。
资料:① Fe,FexCy在加热时与O2反应能生成Fe2O3和CO2。
②FexCy不与酸反应。
实验1:取30.48g样品,加入足量稀H2SO4,充分反应后生成1.00gH2。
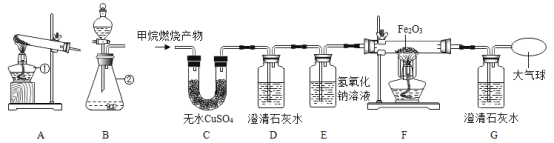
实验2:另取30.48g样品,按下图进行实验。
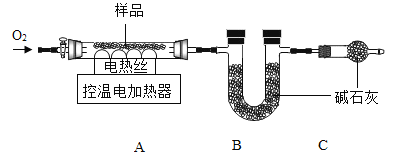
表:装置A和B的质量变化
装置 | A | B |
反应前 | 400.00g | 400.00g |
反应后 | mg | 400.88g |
实验后A中固体全部变为红棕色,装置A、B的质量变化如上表。
(1)装配好装置后,实验前先要____。
(2)装置C的作用是____。
(3)FexCy中,x:y=____。表中m的值是____g。
(实验反思):若用空气(除去CO2)的替代O2进行实验,测得x:y的值偏大,可能的原因是____。
【题目】小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡。为了解其反应过程,他与学习小组的同学进行了如下探究。
(探究一)小组同学根据所学的化学知识设计并进行了如图所示的实验。
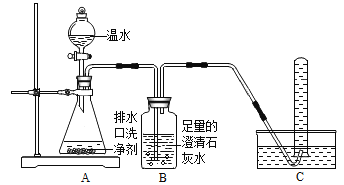
A B C
实验中观察到如下现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺。由此同学们得出结论:生成的两种气体分别是:______(填化学式)。B中有关反应的化学方程式是_____________________________________。
(探究二)
(1)实验过程:
教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:

(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设: 根据以上实验现象,X溶液中一定存在的溶质是________;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种。
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3 + CaCl2 ═ CaCO3↓ + 2NaCl。
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同。
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验。请将下列实验方案填写完整。
实验操作 | 主要实验现象 | 结论 |
① |
| 证明溶液中有Na2CO3 |
② |
| 证明溶液中无NaHCO3 |
③ |
| 证明溶液中无NaOH |
(6)实验反思:根据资料,NaHCO3溶液能与石灰水反应生成白色沉淀。于是,同学们猜想:碳酸氢钠与氢氧化钠是否可以发生__________________________(写方程式)这样的反应?于是,同学们进行了新的探究实验。
【题目】某同学在做铝与酸反应的实验中发现了一个怪现象并记录于下表中,为了探究影响反应速率的因素及两者反应差异的原因,该同学做出了以下假设,你认为假设不合理的是
反应时间 | 1 | 2 | 5 | 15 | 20 | |
实验1 | 质量分数 | 极少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
实验2 | 质量分数 | 无明显现象 | 极少量气泡 | |||
A.与盐酸反应开始产生气泡速率慢的原因:铝片表面有氧化膜
B.与盐酸反应产生气泡速率越来越快的原因:反应放热,溶液温度升高
C.两者反应差异的原因:盐酸中有![]() ,稀硫酸中没有
,稀硫酸中没有![]()
D.两者反应差异的原因:![]() 对反应有促进作用,
对反应有促进作用,![]() 对反应有阻得作用
对反应有阻得作用
【题目】某班同学为验证碳酸钠的化学性质,向盛有碳酸钠的试管中加入一定量的稀盐酸,迅速用带导气管的橡胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中(如图所示)。请回答下列问题:
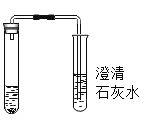
(1)右侧试管中澄清石灰水变浑浊,写出该反应的化学方程式_____。
(2)实验结束后,将两支试管中的所有物质倒入同一个废液缸中,充分反应后得到澄清溶液。同学们对废液中溶质的成分进行如下探究(忽略二氧化碳的影响):
(提出问题)
废液中溶质的成分是什么?
(做出猜想)
猜想一:CaCl2、NaCl和HCl
猜想二:CaCl2、NaCl和Na2CO3
猜想三:_____;
(进行讨论)
经过讨论,同学们一致认为猜想_____是错误的。
(设计实验)请完成实验报告
实验步骤 | 实验现象 | 实验结论 |
取少量废液于试管中,加入_____; | _____ | 猜想一成立 |
(反思拓展)
最终同学们确认了废液中溶质的成分。若将废液直接排入铸铁管道引起的危害是_____,你认为该废液的处理方法是_____。