题目内容
【题目】为了从硝酸亚铁和硝酸银的混合溶液中,提取并回收银,小燕设计了如下的实验方案:
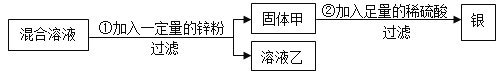
(1)若溶液乙为无色溶液,则固体甲一定含有的物质是_____,可能含有的物质是_____,写出一个在步骤①中肯定发生的反应的化学方程式_____。
(2)若溶液乙为浅绿色溶液,则溶液乙中溶质的组成可能是_____或_____(填物质的名称或化学式)。
【答案】铁、银 锌 Zn+Fe(NO3)2═Zn(NO3)2+Fe(或Zn+2AgNO3═Zn(NO3)2+2Ag) Zn(NO3)2、Fe(NO3)2 Zn(NO3)2、Fe(NO3)2、AgNO3
【解析】
(1)在金属活动性顺序中,锌>铁>氢>银,在硝酸亚铁和硝酸银的混合溶液中,加入一定量的锌,锌先与硝酸银反应生成了硝酸锌和银,若硝酸银完全反应锌再与硝酸亚铁反应生成了硝酸锌和铁,乙为无色溶液,说明硝酸亚铁和硝酸银全部参加化学反应,锌能与硝酸亚铁反应生成硝酸锌和铁,能与硝酸银反应生成硝酸锌和银,故固体甲中含有铁和银,可能有剩余的锌,发生反应的方程式是:Zn+Fe(NO3)2═Zn(NO3)2+Fe、Zn+2AgNO3═Zn(NO3)2+2Ag;
(2)若溶液乙为浅绿色溶液,说明了溶液中含有硝酸亚铁,锌完全发生了反应,溶液中一定含有硝酸锌、硝酸亚铁,可能含有硝酸银。所以溶液乙中溶质的组成可能是Zn(NO3)2、Fe(NO3)2或Zn(NO3)2、Fe(NO3)2、AgNO3。
故答案为:(1)铁、银;锌;Zn+Fe(NO3)2═Zn(NO3)2+Fe(或Zn+2AgNO3═Zn(NO3)2+2Ag)。
(2)Zn(NO3)2、Fe(NO3)2;Zn(NO3)2、Fe(NO3)2、AgNO3。

 每日10分钟口算心算速算天天练系列答案
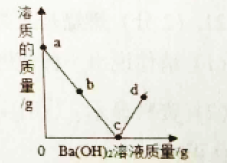
每日10分钟口算心算速算天天练系列答案【题目】某实验小组的同学为了测定CaCl2和NaCl的混合物中CaCl2的含量,他们取样品25.8g于烧杯中,加入134.2g水全部溶解,再多次加入某Na2CO3溶液充分反应。加入Na2CO3溶液 与产生沉淀的质量如下表所示:
Na2CO3溶液/g | 10 | 10 | 10 | 10 | 10 | 10 |
沉淀质量/g | 5 | 10 | 15 | 20 | 20 | m |
(1)Na2CO3中钠、碳、氧三种元素的质量比为_____,表中m=_____。
(2)样品中CaCl2的质量是____;恰好完全反应时,所得溶液中溶质的质量分数是____。
【题目】酱油在使用及储藏过程中颜色会变深,逐渐降低品质。实验小组通过实验研究温度、氧气、光照3个因素对酱油颜色的影响。
(查阅资料)① 通过色差仪检测L*值可监控酱油颜色变化,酱油颜色越深,L*值越小。
② 保鲜瓶具有的特点是挤出盛放的物质后,空气不会进入。
(实验准备)
将等量样品(同品牌、同批次、初始L*值为43.82的酱油)分装到500 mL的不同容器中,密封。
(进行实验)
实验1:将装有样品的多个透明玻璃瓶置于不同温度的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。
编号 | 温度 | 15天 | 30天 | 45天 |
1-1 | 5 ℃ | 43.77 | 43.53 | 42.91 |
1-2 | 28 ℃ | 43.71 | 43.19 | 42.85 |
1-3 | 45 ℃ | 43.67 | 42.55 | 40.89 |
实验2:将装有样品的两个容器置于28 ℃的恒温箱中。每15天,分别倒出100 mL酱油,剩余样品放回恒温箱。用色差仪检测倒出样品的L*值,结果如下。
编号 | 容器 | 15天 | 30天 | 45天 |
2-1 | 透明玻璃瓶 | 43.45 | 42.36 | 41.30 |
2-2 | 透明保鲜瓶 | 43.72 | 42.98 | 42.53 |
实验3:将装有样品的多个容器置于28 ℃的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。

(解释与结论)
(1)实验1得出的结论是_____。
(2)实验2的目的是_____。
(3)实验3欲研究光照对酱油颜色的影响,应选用的容器是_____。
(4)家庭常使用透明玻璃瓶盛放酱油。解释“在相同时间内,使用过的酱油比未开封的酱油颜色深”可依据的实验是_____(填编号)。
(反思与评价)
(5)结合本实验,你对使用或储藏酱油的建议是_____。
(6)酱油在酿造过程中,有时会产生过量的铵盐(如NH4Cl)影响酱油的口感。可用碳酸钠除去铵盐,原理如下,补全该反应的化学方程式。Na2CO3 + 2NH4Cl === 2NaCl + 2NH3↑ + H2O +_____