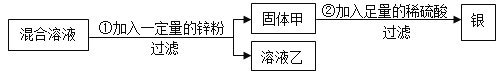
题目内容
【题目】请结合图示实验装置,回答下列问题。
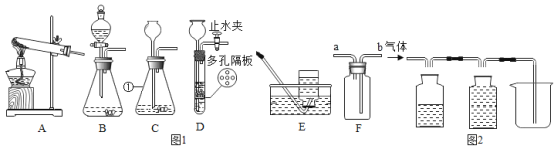
(1)写出标号①的仪器名称:______。
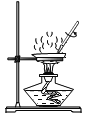
(2)实验室用纯净物加热制取氧气,应选择的发生装置是_____(选填序号),反应的化学方程式为_____。
(3)若选择D装置制取二氧化碳,在反应过程中,使反应停止的操作是______。
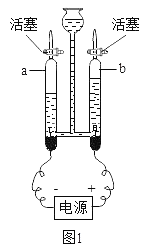
(4)若用E装置收集氧气,当导管口有气泡_____时才能将导管伸入集气瓶中。若用 F 装置收集二氧化碳,气体应从__端通入(选填“a”或“b”)。
(5)实验室用电石(固体,主要成分CaC2)和水反应制取乙炔(C2H2)气体,该反应极剧烈,为控制反应速率,发生装置应选____(填序号).用电石制得的乙炔气体中常混有酸性气体,为了得到较纯净的C2H2,可将气体通过氢氧化钠溶液后,用排水法收集,请在答卷图2将除杂及收集装置补画完整____。
【答案】锥形瓶 A ![]() 关闭弹簧夹 较连续均匀冒出 b B
关闭弹簧夹 较连续均匀冒出 b B 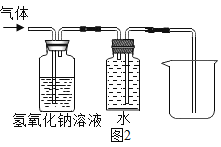
【解析】
(1)据图可知①的仪器名称锥形瓶;
(2)选用纯净物制取氧气,只能是高锰酸钾作为反应物,为固体物质且需要加热,所以选择固体加热装置A;高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气,反应的化学方程式:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)D装置带有活塞,关闭活塞,内部气体增多,压强增大,液体被压入长颈漏斗,固液分离,反应停止;
(4)排水法收集收集气体时,由于内部残留空气的影响,会先形成气泡逸出,此时气泡不连续,不是生成的氧气,待反应一段时间后,氧气输出稳定,形成连续均匀气泡时,氧气才较为纯净,方可进行收集;二氧化碳密度比空气大,进入瓶中先在底部聚集,因此从长口b进气;
(5)反应物为固液混合物,且不需要加热,所以选择固液不加热发生装置,同时需要控制反应速率,因此需要控制反应物浓度,C带有分液漏斗可以控制反应物的量,从而控制反应速率;酸性气体被氢氧化钠吸收,为了充分吸收,需要从长口进气,然后从短口出气,进入盛满水的集气瓶中,乙炔不易溶于水,且密度比水小,因此从短口进气,长口排水,达到收集气体的目的,所以氢氧化钠吸收瓶从长口进气,短口进入盛满水的集气瓶中,短口进入集气瓶,然后长口排出水,达到收集较为纯净的乙炔的目的如图: 。
。