题目内容
【题目】下列图像不能正确反映其对应关系的是
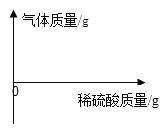
A. 向装有等质量锌、铁的两只烧杯中分别加足量等浓度的稀盐酸
向装有等质量锌、铁的两只烧杯中分别加足量等浓度的稀盐酸
B.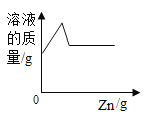 向硝酸银和硝酸铜混合溶液中加入过量的锌粉
向硝酸银和硝酸铜混合溶液中加入过量的锌粉
C. FeCl3和HCl混合液中加入NaOH溶液
FeCl3和HCl混合液中加入NaOH溶液
D.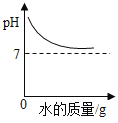 常温下向装有澄清石灰水的烧杯中逐渐加水
常温下向装有澄清石灰水的烧杯中逐渐加水
【答案】AB
【解析】
A、向装有等质量锌、铁的两只烧杯中分别加足量等浓度的稀盐酸,最终铁产生的氢气多;若消耗稀盐酸相同,则生成氢气质量相同,故开始两斜线重合,后因稀盐酸过量,铁消耗稀盐酸多,生成氢气多,拐点高些,故选项图像错误;
B、向硝酸银和硝酸铜混合溶液中加入过量的锌粉,先与硝酸银溶液反应,反应的化学方程式为Zn+2AgNO3═Zn(NO3)2+2Ag,由反应时的质量比可知,每65份质量的锌可置换出216份质量的银,溶液的质量先减少;再与硝酸铜溶液反应生成硝酸锌溶液和铜,反应的化学方程式为Zn+Cu(NO3)2═Zn(NO3)2+Cu,由反应时的质量比可知,每65份质量的锌可置换出64份质量的铜,溶液的质量再增加;完全反应后不再发生改变,故选项图像错误;
C、FeCl3和HCl混合液中加入NaOH溶液,先与氢氧化钠溶液反应,开始时不会生成沉淀,消耗完再与FeCl3反应会生成氢氧化铁沉淀,故氯化铁的质量先不变,滴加一定量的氢氧化钠溶液后,再不断减少,最终减少至0;故选项图像正确;
D、常温下向装有澄清石灰水的烧杯中逐渐加水,但溶液始终显碱性,溶液的pH不可能小于或等于7,故选项图像正确。
故选AB。

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案【题目】做“中和反应”实验时,小聪同学向盛有氢氧化钠溶液的烧杯中滴加稀硫酸,一会儿后发现忘了滴加酸碱指示剂,于是他停止滴加稀硫酸。同学们对反应后溶液中含有哪些溶质展开了讨论。
(提出问题)上述实验中发生反应的化学方程为_____,那反应后溶液中的溶质是什么?
(提出猜想)猜想一:溶质是Na2SO4 猜想二:溶质是Na2SO4 和NaOH 猜想三:溶质是______
(查阅资料)Na2SO4 溶液呈中性
(实验探究)小聪同学设计如下的实验方案
方法步骤 | 实验现象 | 实验结论 | |
方案一 | 取少量烧杯中的溶液于洁净的试管中,滴入几滴无色酚酞溶液 | 酚酞不变红色 | 猜想一正确 猜想二不正确 |
方案二 | 取少量烧杯中的溶液于洁净的试管中, 滴加BaCl2溶液 | 出现白色沉淀 | 猜想三正确 |
方案三 | 取少量烧杯中的溶液于洁净的试管中,加入少量的黑色CuO粉末,振荡 | _ | 猜想三正确 |
(方案评价)同学们对小聪的实验方案讨论后认为:
①方案一存在缺陷,该方案不能证明猜想一是正确的,其原因是___。
②方案二也不能证明猜想三是正确的,理由是___。
③同学们经过讨论,一致认为方案三能够证明猜想三是正确的,并讨论除此方案外,还可以向烧杯的溶液中加入活泼金属或碳酸盐等物质进行证明。
(实验反思)在分析化学反应后所得物质成分时,还需考虑反应物的用量。
【题目】某兴趣小组为了探究一瓶久置的氢氧化钠溶液的变质情况,取出100g该溶液样品进行实验,依次加入质量分数4.9%的稀硫酸,测得的实验数据如下表所示:
实验编号 | ① | ② | ③ | ④ | ⑤ |
稀硫酸的质量(g) | 20.0 | 40.0 | 60.0 | 80.0 | 100.0 |
溶液的总质量(g) | 120.0 | 140.0 | 159.78 | 179.56 | 199.56 |
请回答下列问题:
(1)实验①﹑②没有产生气体的原因是 。
(2)100g溶液样品中碳酸钠的质量 。
(3)计算100g溶液样品中已经变质的氢氧化钠的质量(写出计算过程)
(3)分析实验数据,在图中,画出加入4.9%的稀硫酸质量0—80.0g过程中,产生气体质量对应的变化图,并标注必要的数值。